肌萎缩侧索硬化症:发现早期疾病机制
目前,肌萎缩性侧索硬化症(ALS)还没有治愈方法。然而,情况可能很快就会改变。佛罗里达大学和加州大学圣地亚哥分校(UCSD)的研究人员已经发现了一种蛋白质,在神经疾病的早期阶段已经显示出病理特征。该团队已经在杂志上发表了他们的发现,这可能会导致一种治疗这种疾病的新方法Acta Neuropathologica.
2014年夏天,肌萎缩性脊髓侧索硬化症ALS(肌萎缩侧索硬化症)通过社交媒体运动获得了大量关注。在冰桶挑战中,全球数百万人将一桶桶冰水倒在头上,以模拟因极度寒冷而瘫痪的感觉。在德国,大约有6,000至8,000人患有肌萎缩性侧索硬化症,每年约有2,000例新发病例被诊断出来,这种疾病在短短几年内就被证明是致命的。“ALS是一个运动神经元疾病这意味着它会损害控制我们肌肉的神经细胞,”Beate Winner教授解释道。“在第一阶段,肌肉变弱,然后逐渐消瘦,最终导致患者无法独立吞咽或呼吸。”这一社交媒体活动被用来为ALS研究筹集资金。
通过将细胞重新编程成干细胞来逆转生物钟
Beate Winner是佛罗里达大学罕见神经疾病的干细胞模型教授,干细胞生物学系主任,Universitätsklinikum Erlangen速率疾病中心的发言人。她的实验室调查了引发神经系统神经退行性疾病(如渐冻症)的原因,希望由此发现新的治疗方案。
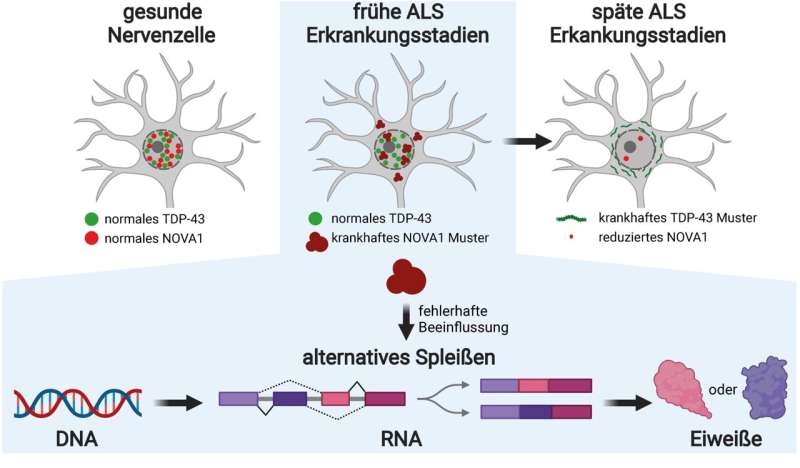
“我们大约15年前就知道,在渐冻人症的末期,患者的病情会恶化蛋白质在神经元中发现的TDP-43变得不溶并开始形成团块,”Winner解释道。“它失去了正常功能,具有毒性。”尽管这些病理变化在患者身上还不明显,但神经细胞的命运已经注定。“我们想知道,在TDP-43改变之前,我们是否能在发展的早期阶段找到ALS的原因。”
她与Jürgen Winkler教授和Universitätsklinikum Erlangen分子神经学系的Martin Regensburger博士一起开始了她的探索。研究人员使用了一种创新技术。他们从肌萎缩性侧索硬化症患者和对照组的健康人的上臂提取了一小块皮肤样本,并将其重新编程为所谓的诱导皮肤多能干细胞这些细胞相当于人类发育的非常早期阶段,理论上可以发育成人体内的任何细胞。这些干细胞然后转化为神经细胞。
温纳解释说:“基本上,我们把时钟往回拨,生成模仿胎儿发育阶段的神经元。”来自成年人的细胞可以重新编程成多能干细胞的事实是由山中伸弥发现的,他的工作获得了诺贝尔医学奖。
NOVA1蛋白在早期就表现出病理特征
埃尔兰根的研究人员使用质谱法(一种高通量程序)在细胞样本中寻找不溶蛋白。他们是成功的。在神经细胞他们发现了一种名为NOVA1的rna结合蛋白。“在神经元中,这种蛋白质表现出了包括无力程度大幅增加在内的变化,但还没有TDP-43的典型病理特征,”佛罗里达大学团队成员、该研究的主要作者Florian Krach博士解释说。“对照组的细胞没有出现这些变化。”
带着这些发现,Krach来到了由巴伐利亚加州技术中心(BaCaTeC)资助的美国加州大学圣地亚哥分校著名RNA生物学家和生物信息学专家Gene Yeo教授的实验室。多亏了专门的实验和计算机辅助分析,他得以研究NOVA1与RNA分子中的什么结合以及它对RNA分子的影响可变剪接在人类神经元。“选择性剪接是一种极其复杂和巧妙的机制,人类用它来增加蛋白质的储备,”克拉奇解释说。“RNA信使分子的部分要么被切断,要么被增加,从而阻碍、扩展或改变蛋白质的功能。”
研究人员希望他们的发现将有助于使早期诊断成为可能,并为新的治疗概念打开大门。
一段时间以来,人们已经知道,ALS患者的替代剪接过程是不受控制的。众所周知,TDP-43也会影响这一过程。然而,来自Erlangen的研究团队怀疑,在TDP-43发生变化之前,其他rna结合蛋白负责疾病早期的病理过程。现在,随着发现NOVA1功能受损,这种怀疑得到了证实。
“我们已经有了一个开创性的发现,但这只是可能能够在早期阶段检测到肌萎缩性侧索硬化症的第一步,”Beate Winner说。“更大规模的后续研究可以加深我们对rna结合蛋白重要性的理解。”研究人员希望他们的工作将有助于在神经元跨越不归点之前开发新的治疗概念。
进一步探索