癌症转移和动脉粥样硬化的共同机制
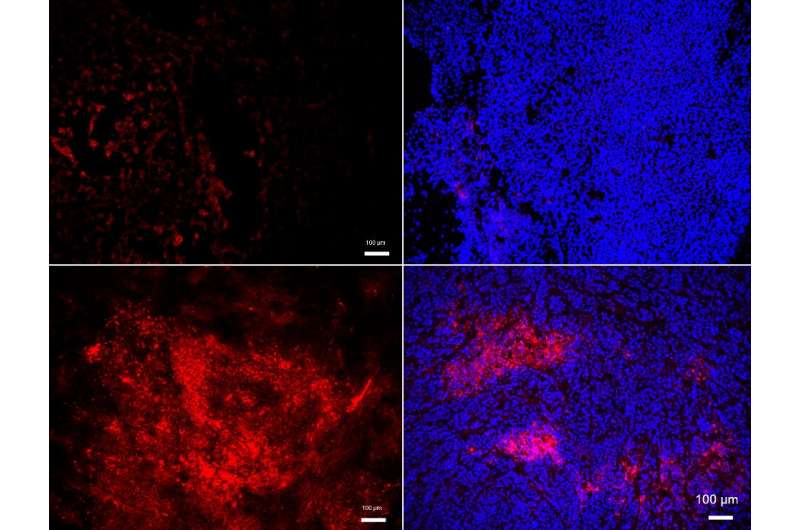
一种癌症转移的关键分子已经被确定为一种已知的参与心血管疾病的分子,这表明一种可能同时治疗这两种疾病的方法。
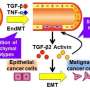
癌症是身体细胞不受控制的生长导致肿瘤的形成,由细胞基因组突变的积累引发。为了变成恶性转移性癌症,肿瘤细胞经历一系列的转化,包括人体免疫系统和肿瘤之间的相互作用。然而,这一过程中的许多机制细节仍不清楚,使得预防和癌症的治疗出了名的困难。然而,越来越多的证据表明,在肿瘤进展到转移的过程中,血管内皮细胞的炎症是一个关键过程。
关注分子机制在恶性肿瘤的这一过程背后,北海道大学Kyoko Hida教授领导的研究小组发现,在恶性肿瘤中,内皮细胞积累了一种称为脂质传递分子低密度脂蛋白(低密度脂蛋白),吸引称为中性粒细胞的免疫细胞。中性粒细胞是免疫抑制细胞,已知有助于肿瘤进展。这一发现发表在《科学》杂志上国际癌症杂志.
该团队之前的工作已经揭示了这一点血管在恶性肿瘤中表达高水平的蛋白聚糖,并且已知癌组织是发炎的。这些特征与动脉粥样硬化的特征相似,研究小组希望研究这种相似性是否更深入。
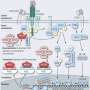
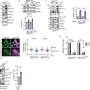
研究小组表明,与非转移性肿瘤相比,转移性肿瘤会积累蛋白聚糖分子;这些物质会附着在血管壁上,并在血管壁上积累低密度脂蛋白。结合的LDL被氧化。在转移性肿瘤的血管内皮细胞中也有高水平的LOX-1受体。他们发现,这会导致这些细胞产生吸引中性粒细胞的炎症信号。他们随后证明,在小鼠中,抑制LOX-1可以显著降低肿瘤恶性程度,而且LOX-1过表达导致吸引中性粒细胞的信号分子增加。
正如研究小组所假设的那样,在恶性肿瘤并不新鲜:它发生在动脉粥样硬化,血管硬化。“动脉粥样硬化和癌症似乎是完全不同的疾病,但它们在血管中有几个共同的病理生理特征,”Kyoko Hida说。
尽管一些问题仍未解决,特别是中性粒细胞如何促进恶性肿瘤的机制,但本研究首次明确证明了心血管疾病与癌症进展之间的机制共性,并追踪了体内肿瘤组织中LDL积累和LOX-1表达的机制。Hida解释说:“我们目前的研究重点是内皮细胞中LOX-1作为癌症和动脉粥样硬化之间的共同因素的重要性。”“肿瘤中中性粒细胞的存在是肿瘤进展的一个显著标志。”
这项研究还指出了一种治疗和预防恶性癌症的有前途的方法心血管病-通过靶向中性粒细胞招募内皮细胞.Hida总结道:“死于心血管疾病而非癌症的癌症患者数量正在增加。靶向LOX-1/氧化LDL轴可能是同时治疗这两种疾病的一种有前途的策略。”
进一步探索