CRISPR技术突出了导致肺气肿和COPD发展的基因
来自波士顿医学中心和波士顿大学医学院再生医学中心的研究人员使用CRISPR的变体来了解导致肺气肿和慢性阻塞性肺病(COPD)的基因的功能。发表在科学的进步在美国,研究人员通过关闭导致这些疾病发病机制的基因表达,发现了功能性后果。
“这是CRISPRi和CRISPRa首次应用于人类诱导多能干细胞了解这些基因的功能作用,”波士顿医学中心肺科医生、波士顿大学医学院副教授安德鲁·威尔逊医学博士说。“这让我们更接近于理解遗传因素如何有助于增加肺气肿的易感性。”
慢性阻塞性肺病和肺气肿是全球第三大死亡原因,造成了严重的疾病负担。肺气肿是一种复杂的遗传疾病,由一些基因的突变或变异引起,导致一些人比其他人更容易患病。全基因组关联研究(GWAS)已经涉及到越来越多的基因中的或附近的变异,但了解它们的功能以及它们如何潜在地促进COPD和肺气肿的发展是相当有限的。
波士顿医学中心和波士顿大学医学院再生医学中心的博士后Rhiannon Werder医学博士说:“目前还没有开发出新的重要药物来帮助治疗全球范围内大量患有COPD或肺气肿的患者。”“我们希望这项研究将有助于了解这种疾病的遗传学,提高我们对这种疾病如何发生的理解细胞水平上并支持开发治疗这些疾病的新疗法。”
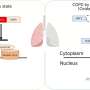
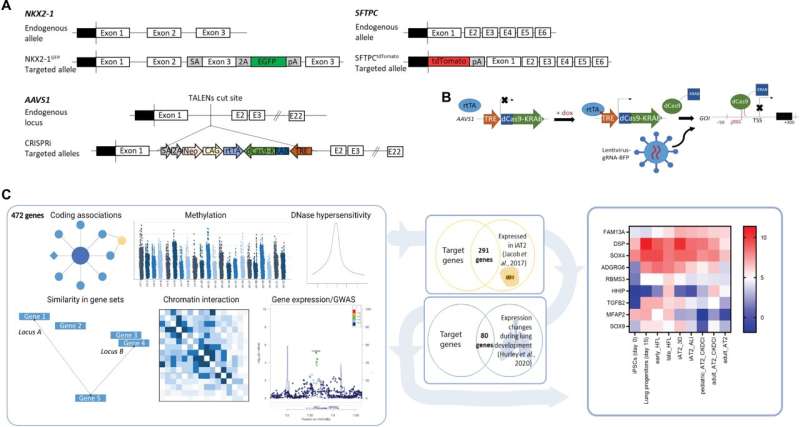
研究人员设计了一种使用CRISPR变体的系统,要么使用CRISPR干扰(CRISPRi)关闭感兴趣基因的表达,要么使用CRISPR激活(CRISPRa)过度表达感兴趣基因诱导多能干细胞(万能)。研究人员在培养皿中培养这些细胞,并对它们进行分化,以生成驻留在肺中的细胞。研究的细胞类型被称为2型肺泡上皮细胞,是肺泡的祖细胞——肺泡是肺中发生气体交换的部分,也是肺气肿中受损的结构。因此,通过了解GWAS基因如何影响2型细胞,研究人员可以开始了解这些基因如何导致影响这些细胞的疾病,如肺气肿。
一旦生成2型细胞,研究人员就使用CRISPRi关闭9种不同的GWAS基因的表达,并分析它们,看看细胞是如何受到影响的,特别是它们的增殖能力,它们需要能够对发生在2型细胞中的损伤做出反应肺气肿.研究人员注意到,关闭一个特定的基因,desmoplakin (DSP),会导致细胞增加增殖,并增加与细胞成熟相关的基因的表达。研究人员发现,在烟雾暴露前关闭DSP表达的细胞中,细胞连接基因的表达比对照组关闭的程度更大。它们也比对照组更善于形成新的菌落,这是衡量祖细胞功能的一个指标。研究人员随后观察了从肺中删除了DSP的小鼠上皮细胞与正常DSP的对照组小鼠相比。研究人员发现,DSP缺失小鼠的2型细胞在损伤后增殖能力更强,这与人类ipsc来源的2型细胞的发现一致。
DSP似乎可以调节2型细胞在基线和损伤后的增殖能力人类疾病,如烟雾暴露。较低水平的DSP表达增加了系统中2型细胞的增殖能力,潜在地使它们能够更好地对损伤做出反应。相比之下,在含有GWAS与COPD风险相关变异的细胞中发现的较高表达水平似乎使细胞在烟雾暴露后增殖能力下降,这可能解释了该基因如何导致疾病。