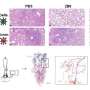
解构骨髓疾病的机制
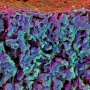
纤维化是由于纤维细胞外基质(ECM)在组织和器官中的沉积而引起的各种组织的增厚,是人体对各种形式损伤的伤口愈合反应的一部分。当伴有慢性炎症时,纤维化会过度发展,产生无法降解的多余疤痕组织。这一过程会在多个器官引起许多疾病,包括吸烟或石棉引起的肺纤维化,酗酒引起的肝纤维化,以及心脏病发作后经常发生的心脏纤维化。纤维化也可能发生在骨髓(BM)中,骨髓是我们一些骨骼内的海绵组织,里面有造血干细胞(hsc),这会导致疤痕和正常功能的中断。
一个例子是被称为“骨髓增生性肿瘤”(MPNs)的慢性血癌,患者可以发展成纤维化BM(骨髓纤维化),破坏血细胞的正常生产。单核细胞是一种属于髓系细胞组的白细胞,在MPN中由造血干细胞过度产生,并有助于BM环境中的炎症(生态位)。然而,如何纤维化骨髓生态位本身影响单核细胞功能和骨髓炎症尚不清楚。
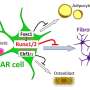
现在,哈佛大学Wyss生物激励工程研究所、John a . Paulson工程与应用科学学院(SEAS)、Dana-Farber癌症研究所(DFCI)和Brigham妇女医院(Brigham)的一个合作团队创建了一个基于可编程水凝胶的体外模型,模拟健康和纤维化的人类BM。他们将该系统与小鼠骨髓纤维化(MF)体内模型相结合,证明单核细胞决定是否进入促炎状态,并根据BM生态位及其密集排列的ECM分子的特定力学特性继续分化为炎性树突状细胞。重要的是,研究小组发现,一种抑制pi3k - γ蛋白的药物淡化了单核细胞的病理机械效应,并减少了它们的数量以及MF小鼠的炎症髓系细胞的数量。研究结果发表在自然材料。
“我们的研究表明,单核细胞的分化状态,这是关键的参与者免疫系统,受到它们遇到的ECM的机械变化的高度调控。具体来说,ECM的粘弹性一直是其机械性能的一个历史上被低估的方面,我们发现在我们的体外和体内模型之间有很强的相关性人类疾病Wyss核心教员David Mooney博士说,他与DFCI研究员Kai Wucherpfennig博士共同领导了这项研究。穆尼补充说:“事实证明,MF是一种与机械相关的疾病,可以通过干扰骨髓细胞中的机械信号来治疗。”
Mooney也是Robert P. Pinkas家族生物工程教授,并领导Wyss研究所的免疫材料平台。Wucherpfennig是DFCI癌症免疫治疗研究中心主任,布里格姆和哈佛医学院神经生物学教授,以及麻省理工学院和哈佛大学布罗德研究所的副成员。Mooney和共同资深作者F. Stephen Hodi博士还领导了免疫工程改善免疫治疗(i3)中心,该中心旨在创建新的基于生物材料的方法来增强对肿瘤的免疫反应。Hodi是DFCI黑色素瘤中心和免疫肿瘤中心的主任,也是哈佛医学院(HMS)的医学教授。
收集机械性骨髓衰竭
大多数生物材料的力学性能是由它们的“粘弹性”特性决定的。与纯弹性物质(如振动石英)不同的是,纯弹性物质在受到机械应力时储存弹性能量,一旦应力消除(缓慢放松),就会迅速恢复到原始状态,粘弹性物质也有粘性成分。就像蜂蜜的粘度一样,这使得它们在机械应变下通过快速应力松弛来消散应力。因此,与慢弛豫的纯弹性材料相比,粘性材料是快弛豫的材料。
该团队开发了一种基于海藻酸盐的水凝胶体系,该体系模仿了天然ECM的粘弹性,使他们能够独立于其他物理和生化特性来调整弹性。通过调整这些人造ECM中弹性和粘性特性之间的平衡,他们可以概括出健康和伤痕累累的纤维化骨髓的粘弹性,其弹性因过量的ECM纤维而增加。放置在这些人造ecm中的人类单核细胞不断地推动和拉动它们,反过来又对材料的机械特性做出反应。
“我们发现,僵硬和更有弹性的缓慢放松的人工ECMs诱导未成熟的单核细胞分化为单核细胞,其促炎程序与MF患者的单核细胞非常相似,并且单核细胞进一步分化为炎性树突状细胞。更粘稠的快速放松的人造ECMs抑制了这种对单核细胞的类似基质的作用,”共同第一作者Kyle Vining博士说,他是Mooney团队的博士后研究员。“这开辟了一种机械检查点的可能性,这种检查点可能在骨髓纤维化骨髓中被破坏,也可能在其他纤维化疾病中发挥作用。”温宁现在是宾夕法尼亚大学预防和修复科学的助理教授。
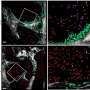
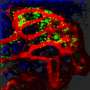
接下来,研究小组研究了刚性和弹性水凝胶的力学特性与实际BM中的力学特性相比如何受到MF的影响。他们利用了一种小鼠模型,在该模型中,一种被称为Jak2的基因的激活突变导致MPN, BM中的促炎信号,以及MF的发展,类似于人类MPN患者的疾病过程。当他们使用纳米压痕探针研究动物股骨中BM的机械性能时,研究人员测量到其硬度高于非纤维性BM。“重要的是,我们发现动物模型中MF的病理分级与粘弹性的变化显著相关,”共同第一作者Anna Marneth博士说,她作为博士后研究员与Brigham和DFCI的首席研究员Ann Mullally博士合作,在小鼠模型中率先进行实验,也是该研究的另一位高级作者。
靶向骨髓机制失调
一个重要的问题是,单核细胞对纤维化BM生态位的机械冲击的反应是否可以作为治疗靶点。研究人员重点研究了磷酸肌醇3-激酶(PI3K)- γ蛋白的一种异构体,这种蛋白在单核细胞和密切相关的免疫细胞中特异性表达。pi3k - γ以调节细胞表面下的细胞硬化丝状细胞骨架的组装而闻名,该细胞骨架在机械应力下膨胀,该团队也在遇到纤维化ECM的单核细胞中观察到这一点。事实上,当他们在坚硬的弹性人造ECMs中添加抑制pi3k - γ的药物时,它减弱了它们的促炎反应,并且当给MF小鼠口服治疗时,显著降低了BM中的单核细胞和树突状细胞的数量。
“这项研究为修改目前难以治疗的纤维化疾病的免疫细胞功能开辟了新的途径。该结果也与具有高度纤维化微环境的人类癌症高度相关,如胰腺癌。”
Wyss创始董事Donald Ingber医学博士说:“这项研究是免疫学和机械生物学之间的一个巨大进步,它显示了如何针对组织的机械环境,而不是疾病的遗传基础,可以潜在地实现新一代强大的治疗干预。”