增强对癌症的免疫反应
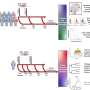
对于淋巴瘤、多发性骨髓瘤或某些类型的白血病患者来说,使用嵌合抗原受体T细胞(CAR - T细胞)治疗有时是战胜癌症的最后机会。这种治疗方法包括从患者血液中提取T细胞,并在实验室中向其添加人工受体car。作为我们免疫系统的守卫,T细胞在我们的血管和组织中进行着永久的巡逻,在那里它们会追捕外来结构。配备了CARs后,T细胞还可以检测到癌细胞非常特定的表面结构。一旦CAR - T细胞通过输注回到患者体内,它们就会作为一种活性药物在体内循环,可以结合非常特定的肿瘤细胞并摧毁它们。
这些工程免疫细胞永久留在体内并繁殖。如果癌症再次发作,它们就会重新发挥作用。至少理论上是这样。但在实践中,许多患者仍然复发。这是因为肿瘤细胞可以通过产生更多的ebag9蛋白来战胜CAR - T细胞,同时也可以使T细胞产生更多的ebag9蛋白。在T细胞中,EBAG9抑制细胞毒性酶的释放,从而减缓所需的免疫反应。
一个月前,Helmholtz协会(MDC)分子医学Max Delbrück中心的Armin Rehm博士和Uta博士Höpken领导的研究小组在《JCI Insight》杂志上发表文章称,关闭小鼠的EBAG9基因会导致对癌症的免疫反应持续增强。小鼠还发育出更多的T记忆细胞。这些细胞是我们免疫记忆的一部分,使我们的免疫系统在之前遇到癌症抗原后能更好地对其做出反应。
现在研究人员也在体外人类CAR - T细胞中展示了这些关键发现。写在分子治疗在美国,该团队表示,这是迈向治疗用途的决定性一步。“关闭EBAG9可以让身体更早、更彻底地消灭肿瘤细胞。除了获得更持久的治疗成功,这也可能创造真正的治愈机会,”Rehm说。
为免疫治疗放松刹车
EBAG9基因一经发现,研究人员就认识到它在癌症中起着重要作用。但花了很长时间才确定这个角色到底是什么。当MDC团队在2009年开始研究时,他们发现没有该基因的老鼠处理细菌和病毒感染的能力比有该基因的老鼠好得多,而且它们形成了更多的T记忆细胞,这在肿瘤生物学中特别有趣。
然后在2015年,主要作者Anthea Wirges博士成功地使用microRNA抑制了EBAG9蛋白的合成。在最新的研究中,她使用microRNA培养不同人类白血病或淋巴瘤细胞的“ebag9沉默”CAR - T细胞。就像在小鼠模型中一样,沉默更能减少肿瘤的生长。复发也是在很久之后才出现的。
“释放EBAG9刹车可以让基因工程T细胞释放更多的细胞毒性物质。然而,它们不会引起CAR治疗的典型副作用——强烈的细胞因子风暴,”Wirges说。事实上,由于使用较少的细胞,这种风险被最小化了。“关闭免疫刹车是全面有效的。我们可以用我们生产的每一个CAR - T细胞来做这件事——不管它针对的是哪种类型的血癌。
下一步是临床研究
然而,血癌的一线治疗仍将是化疗结合传统抗体治疗,因为许多患者对此反应非常好。“CAR疗法只有在癌症复发时才会发挥作用。它非常昂贵,因为它是一个人的单个细胞产品,”Höpken说。用这种产品进行一次治疗就能挽救一条生命。
EBAG9的工作显示了毅力和耐心对研究人员是多么重要。Wirges的动机是她的工作有一个真正的临床应用机会的前景。Rehm补充说:“像这样的项目可以让你在基础研究中掌握一种技术,然后将一切应用到转化研究中——直到毒理学筛选的监管过程。”他们的项目现在已经到了最后一个阶段:研究人员将在11月向德国生物制剂审批机构保罗·埃利希研究所(Paul Ehrlich Institute)提交他们的概念。
多亏了他们在动物模型和使用人体细胞的体外实验中的发现,研究小组现在知道释放EBAG9制动是非常有效的,并且不会比传统的CAR - T疗法产生更多的副作用。“我们现在需要大胆的临床医生和一个合作伙伴来资助临床研究雷姆说。如果一切顺利,使用ebag9沉默的CAR - T细胞的治疗可以在最短的两年时间内用于患者。
进一步探索