科学家发现线粒体DNA与动脉粥样硬化风险增加之间存在惊人的联系
线粒体被认为是细胞的动力源,但越来越多的证据表明,它们也在炎症中发挥作用。来自索尔克研究所和加州大学圣地亚哥分校的科学家在免疫力2022年7月26日,他们检查了人类血细胞,发现了线粒体、炎症和DNMT3A和tet2之间惊人的联系,这两种基因通常有助于调节血细胞生长,但当突变时,与动脉粥样硬化风险增加有关。
“我们发现,基因DNMT3A和TET2,除了它们改变化学标签来调节DNA的正常工作外,还直接激活了一个涉及线粒体炎症途径的基因的表达,这暗示了动脉粥样硬化治疗的一个新的分子靶点,”共同资深作者、索尔克教授、圣地亚哥Nathan Shock基础生物学卓越中心主任Gerald Shadel说。
这项研究始于加州大学圣地亚哥分校的研究人员在研究DNMT3A和TET2突变在克隆造血中的作用时注意到一种特定的炎症反应——当突变未成熟时血细胞产生成熟血统的群体细胞有相同的突变。他们报告说,异常的炎症信号也与血液中DNMT3A和TET2缺乏有关细胞在其中扮演了重要的角色炎症促进动脉粥样硬化进展的反应。
但DNMT3A和TET2基因是如何参与炎症和动脉粥样硬化的尚不清楚。
“问题是,我们无法弄清楚DNMT3A和TET2是如何参与其中的,因为它们编码的蛋白质在DNA调控方面似乎做着相反的事情,”加州大学圣地亚哥医学院的资深合著者克里斯托弗·格拉斯(Christopher Glass)说。“它们的对抗活动让我们相信可能有其他机制在起作用。这促使我们采取了一种不同的方法,并联系了Shadel,他在几年前检查线粒体DNA应激反应时发现了相同的炎症途径。”
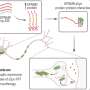
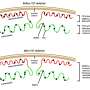
线粒体内存在着细胞DNA的一个独特子集,必须正确地组织和浓缩以维持正常功能。Shadel的团队以前通过移除TFAM来研究线粒体DNA压力的影响,TFAM是一种帮助确保线粒体DNA正确包装的基因。他们发现,当TFAM水平降低时,线粒体DNA会从线粒体排出到细胞内部。这就触发了相同的分子警报,告诉细胞有细菌或病毒入侵者,并触发了促进炎症的防御性分子途径。
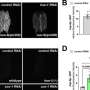
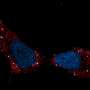
来自Glass和Shadel实验室的科学家们一起合作,以更好地理解为什么DNMT3A和TET2突变会导致类似于线粒体DNA应激时观察到的炎症反应。研究小组应用了基因工程工具和细胞成像技术,对细胞正常、DNMT3A或TET2表达功能突变缺失以及动脉粥样硬化患者的细胞进行了检测。
他们发现,通过实验减少正常血细胞中DNMT3A或TET2的表达,其结果与功能突变和丧失的血细胞相似血细胞动脉粥样硬化患者的炎症反应增加。值得注意的是,血液中DNMT3A和TET2表达水平较低细胞导致TFAM表达减少,进而导致线粒体DNA包装异常,由于线粒体DNA释放,引发炎症。
“我们发现DNMT3A和TET2突变阻止了它们结合和激活TFAM基因的能力,”第一作者Isidoro Cobo说,他是加州大学圣地亚哥分校Glass实验室的博士后研究员。“缺少或减少这种结合活性会导致线粒体DNA释放和过度活跃的线粒体炎症反应,我们认为这可能会加剧动脉粥样硬化中的斑块积聚。”
“我们发现TFAM损耗导致线粒体DNA压力和炎症与动脉粥样硬化等疾病直接相关,这是非常令人兴奋的,”担任生物医学科学奥黛丽·盖泽尔主席的Shadel说。“自从我们揭示了这一途径,人们对参与炎症的线粒体的兴趣激增,许多报告将线粒体DNA释放与其他临床情况联系起来。”
目标疗法炎症许多其他疾病的信号通路已经存在。Glass和Shadel认为,阻断TET2A和DNMT3A突变患者动脉粥样硬化恶化的途径可能成为新疗法的基础。接下来,科学家们将继续研究这一途径,并探索线粒体DNA是如何参与其他人类疾病和衰老的。
其他作者包括索尔克的冈仁波齐·钱德拉·曼加尔哈拉;加州大学圣地亚哥分校的Tiffany N. Tanaka, Addison Lana, Calvin yang, Claudia Han, Johannes Schlachetzki, Jean Challcombe, Bethany R. Fixsen, Mashito Sakai, Rick Z. Li, Hannah Fields, Randy G. Tsai和Rafael Bejar;荷兰威廉敏娜儿童医院的Michael Mokry;阿姆斯特丹大学的Koen Prange和Menno de Winther说。
进一步探索