新的镰状细胞病基因疗法依赖于找到正确的小鼠
镰状细胞病是一种极其虚弱的疾病,影响着非洲国家多达40%的人口,患者会遭受剧烈疼痛、器官损伤和预期寿命缩短的折磨。这种疾病是由制造血红蛋白的基因突变引起的,血红蛋白是在红细胞中携带氧气的蛋白质,受损的血红蛋白会扭曲红细胞的形状,导致疼痛和可能危及生命的血管阻塞。然而,科学家们已经意识到,增加一种健康形式的这种蛋白质(胎儿血红蛋白,通常只在我们在子宫里时产生)的产生,可能为这些患者提供一种革命性的治疗。
在他们的当前疾病模型与机制在这篇文章中,来自美国孟菲斯圣犹大儿童研究医院的Mitchell Weiss和他的同事研究了一种有前景的新治疗方法,该方法正在Weiss的实验室中开发,通过编辑基因来启动成人体内这种健康的胎儿血红蛋白的产生红细胞.在对小鼠进行治疗测试时,研究人员发现,尽管实验室小鼠有镰状细胞病的症状,但胎儿血红蛋白基因和周围的DNA没有正确配置,使得这种革命性的干细胞治疗在动物身上无效甚至有害,这引发了人们对未来在这些实验室小鼠身上测试基于基因的新疗法的担忧。
在一种新的治疗方法在人身上进行试验之前,科学家们先在实验室动物身上进行试验,因此Weiss和同事们在两种携带镰状细胞病症状的老鼠身上试验了他们的新基因疗法:所谓的“伯克利”和“汤斯”老鼠。首先,他们移除干细胞这些干细胞来自小鼠的骨髓,通过编程变成血红细胞,并使用基因编辑修改干细胞的部分DNA,以启动健康的胎儿血红蛋白基因。然后,科学家们把这些重新编程的干细胞放回小鼠体内,并对动物进行了18周的监测,以找出治疗是如何影响它们的。
令人惊讶的是,70%的伯克利小鼠死于这种疗法,而且它只激活了3.1%的小鼠干细胞中愈合胎儿血红蛋白基因的产生。相比之下,实验治疗激活了Townes小鼠57%的红细胞中的胎儿血红蛋白基因,而不影响动物的生存。然而,Townes小鼠红细胞中产生的胎儿血红蛋白水平比用这种方法在实验室培养的人类细胞中观察到的低7到10倍,而且还不够高,不足以减少镰状细胞病的临床症状。
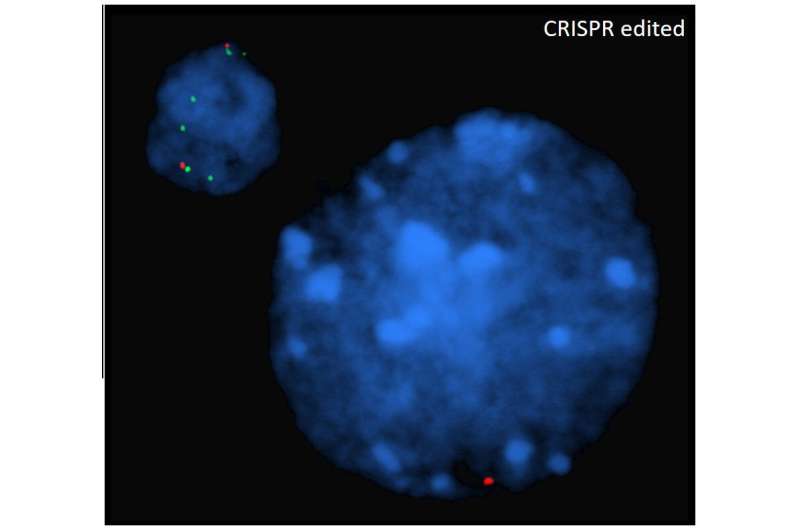
Weiss和他的同事随后想要找出为什么这种新疗法在伯克利小鼠身上没有成功,伯克利小鼠已经被用于测试镰状细胞病的治疗方法几十年了。韦斯博士说:“我们意识到,我们对这些老鼠的基因结构了解不够。”因此,研究小组对伯克利实验鼠的血红蛋白基因和周围DNA进行了测序,发现这些实验鼠并非只有一个突变的人类基因拷贝,而是有22个随机排列的、破裂的突变的人类镰状细胞病基因拷贝和27个人类胎儿血红蛋白拷贝,该研究小组本希望通过激活这些基因来治愈小鼠的镰状细胞病。当科学家们在伯克利实验鼠身上测试基因疗法时,这种复杂的基因构成导致了致命的影响,因为编辑一个基因的多个副本会破坏DNA。这意味着研究人员不能使用这些老鼠来测试和优化这种基因编辑治疗。
相比之下,Townes小鼠只有突变的人类血红蛋白基因和制造人类胎儿血红蛋白的基因的单一副本。然而,这些小鼠可能缺乏通常调节人类胎儿血红蛋白基因产生的关键DNA片段。因此,他们无法产生足够的这种健康蛋白质来缓解老鼠的症状。
Weiss博士评论道:“我们的发现将帮助使用伯克利和Townes小鼠的科学家决定使用哪一种来解决他们的特定研究问题镰状细胞病或血红蛋白。此外,这项工作也提醒科学家们要仔细考虑老鼠他们正在用它来研究人类疾病,并找到适合这项工作的老鼠。”
进一步探索