衰老的心脏会积累突变,同时失去修复它们的能力gydF4y2Ba
为什么患心脏病的风险会随着年龄的增长而上升?高血压或高胆固醇等已知的危险因素并不能解释所有的病例。波士顿儿童医院的一项首次研究表明,组成我们心肌的细胞随着时间的推移会积累新的基因突变,同时失去修复它们的能力。gydF4y2Ba
研究结果发表在该杂志上gydF4y2Ba自然老化gydF4y2Ba.gydF4y2Ba
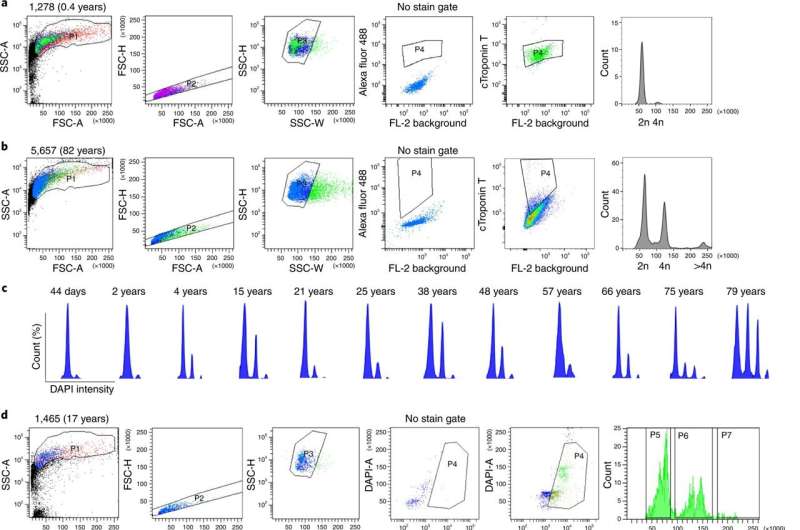
该研究小组由波士顿儿童医院遗传学和基因组学部门的Sangita Choudhury博士和August Yue Huang博士领导,对56个个体的整个基因组进行了测序gydF4y2Ba心肌gydF4y2Ba被称为心肌细胞的细胞来自12个不同年龄段的人——从婴儿到82岁——他们死于与疾病无关的原因gydF4y2Ba心脏病gydF4y2Ba.gydF4y2Ba
记录衰老心脏的突变gydF4y2Ba
利用复杂的生物信息学技术和分析,研究小组比较了非遗传突变的数量gydF4y2Ba体细胞突变gydF4y2Ba研究人员还在不同年龄的细胞中寻找突变模式或“特征”,这些突变模式或“特征”可能阐明癌症的机制gydF4y2Ba心gydF4y2Ba疾病。gydF4y2Ba
“这是第一次在单细胞水平上观察人类心脏的体细胞突变,”乔杜里说,他是这篇论文的共同第一作者。gydF4y2Ba
细胞年龄越大,DNA中的单个“字母”变化(称为单核苷酸变异)就越多。这些突变的模式表明,其中许多是由氧化损伤引起的。gydF4y2Ba
“因为心脏一直在跳动,它消耗了大量的能量,”医学博士、医学硕士陈明辉(音译)解释道,他是波士顿儿童医院遗传与基因组学部门和心脏病学系的心脏病专家。“这gydF4y2Ba能源生产gydF4y2Ba产生称为活性氧或ROS的化学副产物。当ROS水平过高时,它们会破坏DNA。”gydF4y2Ba
雪上加霜的是,突变还影响了细胞通常用来修复DNA损伤的途径。乔杜里说:“修复DNA损伤的机制也受到年龄的影响。”“如果有足够的氧化损伤,这些可能会不堪重负。”gydF4y2Ba
这项技术上困难的研究利用了单细胞gydF4y2Ba全基因组测序gydF4y2Ba以及波士顿儿童医院克里斯托弗·沃尔什(Christopher Walsh)医学博士实验室(Choudhury和Huang都是该实验室的成员)首创的生物信息学技术。沃尔什实验室最近使用这种方法记录了阿尔茨海默病患者神经元中突变的积累。gydF4y2Ba
通常情况下,不继续分裂的细胞,比如心脏细胞,不太容易发生突变。但研究人员发现,心肌细胞积累突变的速度与某些分裂细胞类型一样快,甚至更快;研究人员计算出,每个细胞平均每年有100多个新突变。gydF4y2Ba
“心脏细胞积累突变的速度也比神经元快三倍,神经元是另一种不分裂的细胞类型,”黄说。gydF4y2Ba
除了DNA修复途径外,突变还会影响细胞骨架中的基因,细胞骨架是赋予细胞结构的支架,以及其他基本细胞功能。gydF4y2Ba
“随着年龄的增长,基因突变越来越多,就会产生有害影响,可能会把心脏推到一个临界点,导致疾病,”陈博士说,她与沃尔什和恩jung Alice Lee博士共同担任这项研究的高级研究员。“这可能会导致大量DNA受损,心脏无法正常跳动。”gydF4y2Ba
更多探索gydF4y2Ba
研究人员指出,他们的研究只寻找了单核苷酸变异,并没有调查其他类型的突变,如DNA插入或缺失。另外,因为他们研究的是健康的心脏gydF4y2Ba细胞gydF4y2Ba在美国,他们无法确定这些突变与心脏病有关。在未来,他们计划观察gydF4y2Ba突变gydF4y2Ba来自不同心血管疾病患者的组织gydF4y2Ba
Chen研究癌症的胸部放疗和化疗如何影响心脏健康,他计划收集患有心脏病的癌症患者的数据。gydF4y2Ba
乔杜里补充说:“我们还想研究心脏中不同类型的细胞。”“我们只触及了冰山一角。”gydF4y2Ba
进一步探索gydF4y2Ba