靶向癌症疫苗消除了肿瘤并防止小鼠复发
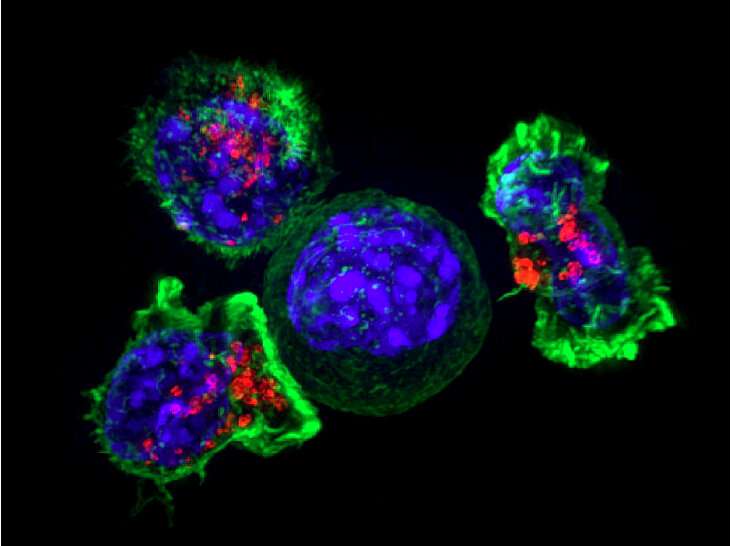
世界各地的研究人员多年来一直致力于开发针对不同类型癌症的疫苗,但没有成功。现在,塔夫茨工程研究人员认为他们找到了一个确实有效的方法。他们设计了一种靶向癌症的方法,该疫苗是如此强,精确,它消除了肿瘤,甚至可以防止其复发。
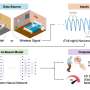
癌症疫苗的作用与辉瑞和现代的共vid疫苗相似,这些疫苗在微小的脂质(FAT分子)气泡中传递mRNA,最终与体内细胞融合,从而使细胞“读取” mRNA并产生病毒抗原,并产生病毒抗原,这些抗原,小片段激活该病毒免疫系统。
癌症疫苗还会在微小的气泡中传递mRNA,但在癌细胞和称为脂质纳米颗粒的气泡可以在淋巴系统-在哪里免疫细胞是“受过训练”的 - 这样的响应更加有效。
生物医学工程学教授Qiaobing Xu说:“我们现在正在做的是使用脂质纳米粒子递送技术开发下一代mRNA疫苗,具有针对特定器官和组织的能力。”“针对淋巴系统,有助于我们克服许多在开发癌症疫苗方面面临的挑战。”该研究在杂志上报道了美国国家科学院论文集。
迄今为止,已有20多种mRNA癌症疫苗已参加临床试验,但通常大部分mRNA最终出现在肝脏中。尽管肝脏中产生的抗原仍然可以诱导免疫反应,但仍有肝炎和损伤的风险。如果将更多的疫苗定向到淋巴系统,该反应可能更有效,持久,其中B细胞,T细胞和免疫系统的其他细胞被浓缩并学会抵抗不受欢迎的入侵者。
Xu和他的团队以前曾设计了脂质纳米颗粒(LNP),该脂肪纳米颗粒针对基因编辑包至脑和肝, 也肺的基因治疗扭转在鼠标模型。通过修改构成气泡以及其他添加剂的脂质的化学结构来实现靶向,直到研究人员找到一种组合,而更喜欢进入感兴趣的器官。在这种情况下,他们发现了一个LNP,该LNP皮下注入小鼠后,该LNP集中在淋巴结中。研究人员认为LNP从血流在它们的表面上,这些选定的分子与靶器官中的特定受体结合。
发现辉瑞联合-19疫苗中使用的当前LNP有利于通过四对一的比例向肝脏与淋巴系统递送。塔夫茨(Tufts)团队逆转了他们的新型LNP的选择性,更喜欢淋巴输送,而不是三对一的比例。
淋巴系统包括在感染期间经常膨胀的熟悉淋巴结,是疫苗的重要靶标,因为这是对外抗原的免疫力,或者在这种情况下是一种癌症抗原。如果将人体视为战场(加性病毒,细菌,寄生虫和肿瘤),而B细胞和T细胞则是士兵,那么淋巴结是训练营,B细胞和T细胞受过训练以更像对敌人有效。
该训练的一个关键要素是树突状细胞和巨噬细胞的参与,即免疫系统的“钻孔中士”,将抗原引入T和B细胞并有助于将其发射。
随着更多的疫苗进入淋巴结,塔夫茨研究人员发现,大约三分之一的树突状细胞和巨噬细胞吸收了癌症疫苗。这比传统疫苗所获得的意义要大得多,而更多的“钻探中士”意味着训练有素的B和T细胞“士兵”,以及对携带与疫苗相同抗原的肿瘤的更有效反应。
这正是研究人员发现的。老鼠与转移性黑色素瘤用淋巴靶向疫苗治疗的肿瘤的显着抑制作用和40%的完全反应发生率(没有肿瘤),从长期中没有复发,当它与另一种现有疗法结合在一起,该治疗有助于防止癌细胞抑制抑制癌细胞免疫反应。
所有完全缓解的小鼠都可以防止任何新的肿瘤在稍后注射转移性肿瘤时形成细胞,表明癌症疫苗导致了出色的免疫记忆。
“癌症疫苗一直是一个挑战免疫反应”塔夫茨大学博士后研究员Jinjin Chen说,他是Qiaobing Xu研究团队的成员。癌症疫苗唤起更强的反应,并能够携带大型和小抗原的mRNA。我们希望它不仅可以成为癌症疫苗的通用平台,而且还可以针对病毒和其他病原体的更有效的疫苗。”
进一步探索