氧化碳气体增加光照疗法在温和的温度
癌症高热光照疗法(PTT)是一种安全的策略,利用光热光谱分析转换代理将光能量转化为热量切除癌细胞。
一方面,高温(> 50℃)PTT周围的健康组织造成不可避免的威胁,可能诱发炎性疾病,因为很难阻止热扩散。另一方面手,烧蚀效应在相对低温(< 45℃),是远远不够的由于调节热休克蛋白的表达(休克),修复热受损细胞,导致肿瘤细胞在激光辐照的耐热性。必须开发新战略为低温PTT休克沉默。
现在,由Cai林涛博士领导的一个研究小组从深圳先进技术研究院(SIAT)中国科学院报告了一个新的策略使用氧化碳气体抑制热休克的表达,为提高低温PTT提供另外一个策略。
该研究发表在《应用化学国际版7月15日。
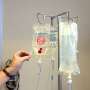
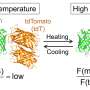
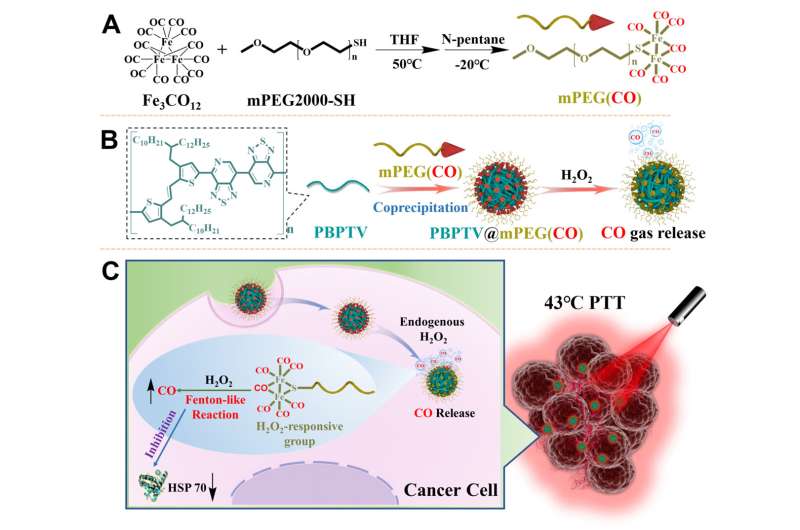
在实验中,研究人员开发了一个chemiexcitation-triggered photo-active nanodelivery系统(称为AIE nanobomb)基于NIR-II发光聚合物的自组装与aggregation-induced发射特性(PBPTV)和自制的一氧化碳(CO)载体聚合物mPEG (CO)。nanobomb可能引发的高水平的H2O2在肿瘤微环境在肿瘤细胞有选择性地释放CO气体。
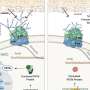
在肿瘤微环境,over-secreted H2O2弥漫整个nanobomb优先分解成·哦激进分子的催化下通过Fenton-like反应,所以和强烈氧化·哦激进分子进一步氧化和竞争性与铁中心协调,导致释放铁中心有限公司。逐步释放公司能有效地抑制热休克摧毁肿瘤的高表达在低温PTT过程中热阻和诱导肿瘤细胞凋亡。
“作为一个安全的治疗模式,光照疗法在温和的温度不仅可以诱导肿瘤细胞凋亡,但也激活免疫系统攻击残留肿瘤细胞在人体和消除肿瘤复发,“蔡博士说。“我们把这里叫做photo-immuno-therapy治疗。毫无疑问,如何选择性地抑制的表达热休克蛋白在肿瘤细胞和反向耐热性细胞是关键。”
小分子热休克抑制剂和携带RNA (siRNA)广泛与光热光谱分析同行并装转换剂来改善低温PTT的治疗效果。小分子热休克抑制剂抗生素或抗癌剂,如tanespimycin(也称为17-AAG),藤黄酸等等。
“他们几乎很难在水中溶解和副作用正常细胞,核似乎是一个不错的方法。然而,它们很容易在人体退化,”张Pengfei博士说,这项研究的主要贡献者,“我们也惊讶,碳氧化物的作品。它激励着我们,没有什么是不可能的。”
“作为信号分子,碳氧化物(CO)可以触发一系列的细胞保护机制在压力和炎症。公司的机制调节热休克蛋白质仍不清楚,”龚萍龚博士说,这项研究的另一个主要贡献者,“根据一些文献,我们可以假设它可能与LKB1 / AMPK / mTOR通路,但仍需要做大量工作来证明这一点。”
PBPTV是一个两极pyridal thiadiazole-based半导体聚合物,bis-pyridal-thiadiazole单元的使用使PBPTV达到高的电子亲和能,低LUMO水平,延长π-conjugation,已经显示出巨大的潜力在有机电子半导体设计高性能的电子传输。
“之前我们从未想过它会发光,并可用于生物医学从来没有想过它。这项工作给我们的承诺我们的材料。跨领域工作我觉得是很重要的,我将继续与该研究小组在SIAT,“陈华捷从湘潭大学博士说,这项工作的合作者。
“气疗法是一个新兴的和有前途的领域,虽然有一些报道与图片结合气体治疗治疗癌症。气体和生物过程之间的相互作用可能会打开新的门来解决现有的一些问题在疾病治疗。除此之外,也有基于气体疗法临床报告。用天然气来解决这个问题照片治疗药物再利用也是一个很好的例子,“蔡博士说。