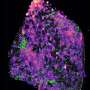
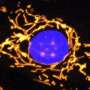
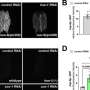
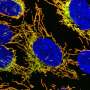
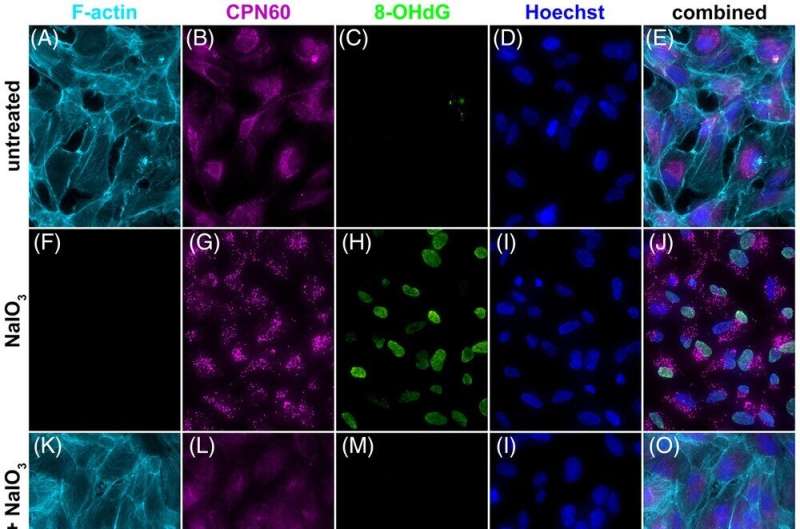
 NaIO对ARPE19细胞的保护作用3..5.0 × 104ARPE19细胞在播种后5小时被AAV2/8-ophNdi1转导;Moi = 5.4 × 105(k o)。转染28小时后,用5-mM NaIO对细胞进行侮辱3.(F-O)和24 h侮辱后细胞固定,用Phalloidin-iFluor 647 (F-actin,浅蓝色)、CPN60(线粒体标记物,紫红色)和8-OHdG-Alexa Fluor 488(氧化应激标记物,绿色)免疫细胞化学染色;核用Hoechst反染色(核染色,深蓝色)。aav2 /8- ophndi处理和NaIO3.-侮辱细胞(K-O)与未处理细胞(A-E)、未处理细胞和NaIO进行比较3.-受辱细胞(F-J)。ophNdi1的表达提供了明显的拯救,因为用病毒处理的受侮辱细胞与未处理的对照细胞具有相似的表型。比例尺(O): 25 μm。(P和Q) 5.0 × 104ARPE19细胞被植入XFe96海马板(n = 3)。第二天至少有5个孔被AAV2/2-ophNdi1 (MOI = 3.4 × 10)转导5).转染28小时后,转染的细胞和至少16孔未转染的细胞被5-mM NaIO侮辱3.侮辱后12 h细胞用XFe96海马进行线粒体应激测试。(P)基础和最大耗氧率(OCRs)、备用呼吸能力(SRC)和ATP生成。(Q)鱼藤酮治疗后AAV2/2-ophNdi1对OCR的挽救也被指出。ocr被归一化为蛋白质。NaIO3.与未受侮辱的细胞相比,侮辱显著减少了基础OCRs、最大OCRs、SRC和ATP的产生(减少66.0%,p < .05;69.8%, p < .01;74.4%, p < .001; 62.1%, p < .05)。值得注意的是,由于ophNdi1表达引起的基础OCR增加大于最大OCR的增加,AAV2/2-ophNdi1进一步降低了SRC(最大OCR与基础OCR的差异)。OCR归一化为蛋白质。*p < .05;**p < .01;***p < .001;2-sample t检验。信贷:临床和转化医学(2022)。DOI: 10.1002 / ctm2.952
NaIO对ARPE19细胞的保护作用3..5.0 × 104ARPE19细胞在播种后5小时被AAV2/8-ophNdi1转导;Moi = 5.4 × 105(k o)。转染28小时后,用5-mM NaIO对细胞进行侮辱3.(F-O)和24 h侮辱后细胞固定,用Phalloidin-iFluor 647 (F-actin,浅蓝色)、CPN60(线粒体标记物,紫红色)和8-OHdG-Alexa Fluor 488(氧化应激标记物,绿色)免疫细胞化学染色;核用Hoechst反染色(核染色,深蓝色)。aav2 /8- ophndi处理和NaIO3.-侮辱细胞(K-O)与未处理细胞(A-E)、未处理细胞和NaIO进行比较3.-受辱细胞(F-J)。ophNdi1的表达提供了明显的拯救,因为用病毒处理的受侮辱细胞与未处理的对照细胞具有相似的表型。比例尺(O): 25 μm。(P和Q) 5.0 × 104ARPE19细胞被植入XFe96海马板(n = 3)。第二天至少有5个孔被AAV2/2-ophNdi1 (MOI = 3.4 × 10)转导5).转染28小时后,转染的细胞和至少16孔未转染的细胞被5-mM NaIO侮辱3.侮辱后12 h细胞用XFe96海马进行线粒体应激测试。(P)基础和最大耗氧率(OCRs)、备用呼吸能力(SRC)和ATP生成。(Q)鱼藤酮治疗后AAV2/2-ophNdi1对OCR的挽救也被指出。ocr被归一化为蛋白质。NaIO3.与未受侮辱的细胞相比,侮辱显著减少了基础OCRs、最大OCRs、SRC和ATP的产生(减少66.0%,p < .05;69.8%, p < .01;74.4%, p < .001; 62.1%, p < .05)。值得注意的是,由于ophNdi1表达引起的基础OCR增加大于最大OCR的增加,AAV2/2-ophNdi1进一步降低了SRC(最大OCR与基础OCR的差异)。OCR归一化为蛋白质。*p < .05;**p < .01;***p < .001;2-sample t检验。信贷:临床和转化医学(2022)。DOI: 10.1002 / ctm2.952
都柏林三一学院的研究人员开发了一种新的基因治疗方法,有望治疗干性老年性黄斑变性(AMD),这是一种进行性眼病,在65岁以上的成年人中影响高达10%,是该年龄组严重视力损害和失明的主要原因。
干性AMD病例约占所有AMD病例的85-90%,目前尚无治疗或预防方法疾病进展,强调了为这种使人衰弱的疾病开发治疗方案的必要性。在成人中,许多老年性疾病已被发现存在线粒体功能缺陷,包括AMD。
三一学院遗传与微生物学院的研究小组开发了一种新的基因疗法(ophNdi1),这是同类疗法中首次直接针对AMD中功能异常的细胞中的线粒体功能。线粒体被称为细胞的“发电站”,因为它们管理能量的产生,但在干性AMD中,它们的性能会大幅下降,这与视力下降有关。
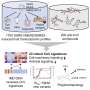
这种新的基因疗法巧妙地利用一种病毒进入正在遭受痛苦的细胞,并传递给失败的线粒体所需的代码,使它们能够产生额外的能量,并继续维持视力。该疗法已在多种干性黄斑变性模型中显示出益处,为有朝一日发展成一种可以帮助全球数百万人的治疗方法带来了希望。
资深作者Jane Farrar教授说:“关键是,这项研究在模型中提供了第一个证据,直接调节眼细胞中的生物能能提供益处,并改善干性AMD的视觉功能。在这样做的过程中,这项研究强调了细胞的能量发电厂线粒体是干性AMD的关键目标。”
三一学院遗传与微生物学院的第一作者兼研究员索菲亚·米林顿-沃德博士说:“我们为干性AMD探索的针对细胞能量或线粒体功能的新型基因疗法在测试的模型系统中始终提供了益处。许多视网膜细胞对视觉至关重要,与大多数其他细胞相比,它们需要特别高水平的能量,这使得它们特别容易受到线粒体功能障碍.我们正在开发的疗法直接针对线粒体功能,并增加视网膜中的能量产生水平,这导致干性AMD疾病模型中更好的视觉功能。
“尽管在将其作为一种治疗方法用于患者之前还有进一步的工作要做,但研究结果给了我们希望,我们正在接近解决这种具有挑战性的、使人衰弱的疾病。”
这项研究刚刚发表在临床和转化医学.
更多信息:Sophia Millington‐Ward等人,AAV介导的基因治疗改善线粒体功能,对年龄相关性黄斑变性模型有益,
临床和转化医学(2022)。
DOI: 10.1002 / ctm2.952
引用:新的基因疗法有望治疗年龄相关性黄斑变性(2022,8月25日),检索自2022年9月29日//www.pyrotek-europe.com/news/2022-08-gene-therapy-age-macular-degeneration.html
这份文件受版权保护。除为私人学习或研究目的而进行的公平交易外,未经书面许可,不得转载任何部分。内容仅供参考之用。