基因检测在怀孕前在近亲夫妻发现更为有效
准父母携带遗传风险的严重疾病,他们有可能遗传给孩子们吗?在美国,医生建议夫妇尝试怀孕前遗传筛查。苏黎世大学的研究人员已经表明这个测试的最大变异检测的风险44%的夫妇是血缘关系,和其他在只有5%的夫妇。在职新获得的突变检出率降低的主要原因是后者。
在怀孕期间使用生物标记和基因检测是现在非常普遍。但如果父母双方的基因进行了广泛的分析可能的风险概念之前?基因组中有罕见的遗传疾病,父亲或母亲在不知情的情况下携带吗?如果父母双方有相同的遗传缺陷在他们的基因,把这个孩子,这往往会导致孩子有严重的疾病。
在美国的许多地方,广泛基因检测提供前瞻性的父母,通常还建议在怀孕早期。检查主要是表明隐性遗传基因性别不明具体句话说,那些有影响只有两个携带突变基因副本。隐性基因位于X染色体上是一个特例,即健康的母亲可以将这种基因传给她们的孩子。然而,通常只有儿子患有这种突变的后果,因为他们只有一个X染色体,因此没有第二个基因复制来弥补这个缺陷。
3000多个遗传因素的考验
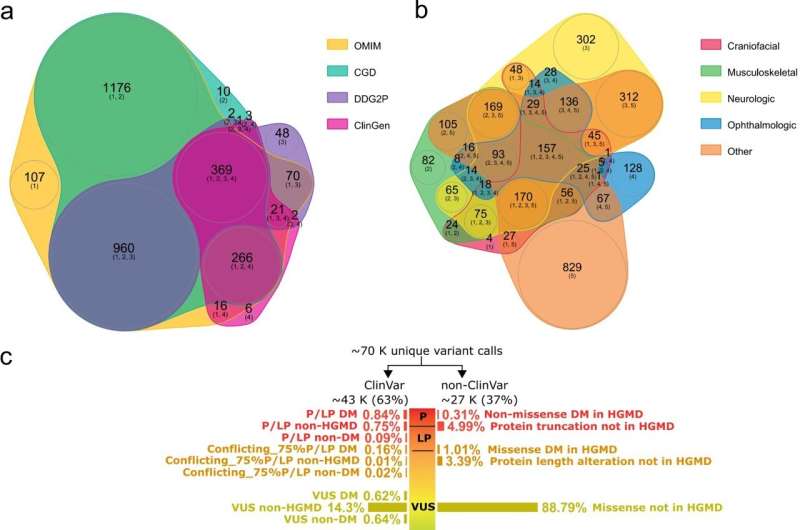
这些遗传基因测试风险因素能兑现承诺呢?主任安妮塔·劳赫苏黎世大学医学遗传学和她的团队首次在瑞士已经解决了这个问题通过广泛研究的潜力和陷阱扩大载体筛查(ECS)。为此,科学家们测试序列数据从700年的父母已经神经发育障碍的儿童。许多超过3000调查基因会导致智障,发育障碍、自闭症和其他障碍。
“在我们的研究中,我们能够表明,这种类型的广泛的基因检测可以检测孩子有严重的发育障碍的风险在大约44%的情况下如果父母被血相关实例作为第一或第二个堂兄弟,”安妮塔·劳赫说。在一些人群这是很常见的,例如在中东和北非。
尤其是缺口风险检测non-consanguineous夫妇
测试还发现约5%的病例的夫妇没有血液相关但只有在所有已知的隐性基因。然而,根据美国建议non-consanguineous夫妇只能检测已知常见基因特定的载波频率的人口。”后,美国建议将减少一半以上风险检出率,因为罕见的基因也起到了一定作用,”劳赫解释道。
non-consanguineous夫妇的孩子,一个更高比例的发展障碍是由在职新创突变,而在父母的孩子是相互关联的遗传基因缺陷扮演更重要的角色。出于这个原因,研究人员状态,检测的可能性风险通过分析non-consanguineous夫妇的父母的基因是有限的。
许多致病基因仍然没有检测到
进一步的潜力因素也影响这些测试在已知致病基因检测有问题的基因变异:特别是,错义突变的基因,基因蓝图的可能或不可能被改变,继承了人类基因组变异,基因副本的数量是不正确的,有被低估了。不能被探测到的情况下一般都是那些在一个继承和新收购的遗传缺陷发生在同一时间。
此外,还有可能至今几千鉴定基因也可能导致发育障碍。为例,在调查研究对象、发展障碍的原因在各自的孩子保持在大约58%的情况下无法解释。
有意识的决定支持或反对孩子
不过,研究人员称,这项研究提供了数据如何有意义的扩展载体筛查。基于血缘的父母容易被探测率高,研究人员认为,筛选当然应该给这样的夫妇。在所有其他情况下,应该权衡利弊在个案基础上,以避免产生不切实际的期望。“如果发现一对夫妇生孩子的风险神经发育障碍,他们将充分认识到,能够决定是否要孩子一起考虑产前或胚胎植入前的诊断,“劳赫说。
然而,结果还表明,减少潜在风险很大程度上取决于所选择的基因和变异测试的分类。根据劳赫,仍有潜力改善测试提供了目前:“提高临床受益,所有的夫妻都应该考虑,想要一个广泛的基因测试筛选所有的隐性基因无关的人口基因变体的患病率。实验室时也应该使用合理的阈值对遗传缺陷被认为是致病”。
这项研究发表在npj基因组医学。
进一步探索