肠道和肺类器官为先天免疫细胞疗法打开了大门
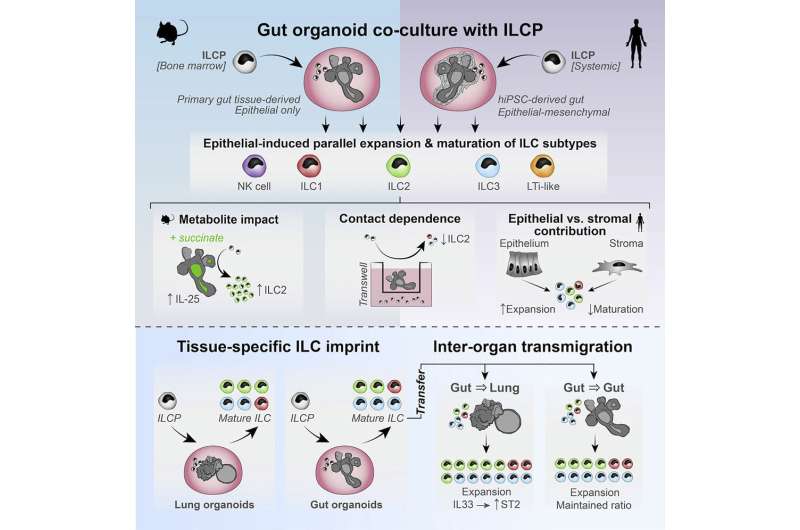
国王学院的研究人员发现了一种在培养皿中扩展和成熟先天免疫细胞的创新方法。
这一发现提供了一个飞跃人类细胞旨在对抗慢性炎症疾病的治疗策略。
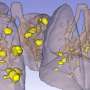
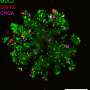
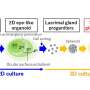
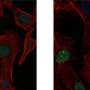
这项技术由伦敦国王学院的Joana F. Neves博士领导,并于今天发表在细胞的报道,使用迷你肠道和肺类器官,意外地证明是上皮细胞驱动组织特异性先天淋巴细胞(ILC)的发展。
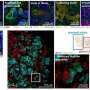
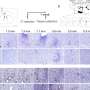
作为她在国王学院的博士研究的一部分,Geraldine Jowett博士利用这个系统表明,当与这些类器官培养时,所有ILC亚群都可以同时成熟和指数增长,当基质细胞耗尽时,这一过程会显著改善,颠覆了基于基质喂养细胞不朽的金标准方法。
现在是剑桥大学(Cambridge University)施密特科学研究员(Schmidt Science Fellow)的乔伊特博士指出,人体实验结果是多么出人意料:“我们在小鼠仅上皮系统中的发现非常稳健和可复制,但在项目早期,人类干细胞衍生的肠道类器官共培养永远无法与小鼠模型的效率竞争。当我们开发间充质耗尽步骤时,我们诚实地预期非上皮部分将比上皮类器官表现更好,作为不朽的间充质细胞是体外ILC研究的金标准。”
“上皮细胞的影响真的让我们大吃一惊。我们从老鼠的实验数据中怀疑上皮细胞对于组织特异性ILC印迹很重要,但我们绝不会认为它们是比肠间质更大的成熟驱动力。这种发现让类器官研究变得如此有趣和有意义,”杰拉尔丁·乔伊特博士说。
该研究形成了一个基础专利申请伦敦国王学院最近提交的申请,其目标是包含这种令人兴奋的驱动先天淋巴细胞成熟的新方法。
这种细胞类型在肠道、肺和皮肤等屏障组织中富集,在这些组织中,它调节体内平衡、对感染的快速反应、癌症监测和组织再生。这些免疫细胞是非抗原特异性的,但产生大量的细胞因子,使它们成为细胞治疗方法的一个有吸引力的靶点。但是,将它们扩展到人体在足够的数量已经证明是这一应用的瓶颈。
该研究的共同资深作者Joana F Neves博士解释说:“我们在8年前就开始了这些研究,当我们观察到类器官驱动的免疫细胞在人类类器官中如此有效时,我们非常高兴。这为对这些罕见但重要的物种进行详细研究开辟了一条途径免疫细胞并有潜力用于这些细胞的扩增,用于自体细胞治疗。”
作者希望这个人类瀑样该系统可以提供一个重要的进展,不仅对我们对固有淋巴样细胞如何在远端粘膜发育的基本理解,而且可以将它们作为炎症的强大调节器。
进一步探索