辉瑞要求欧盟药品监管机构批准调整后的新冠疫苗
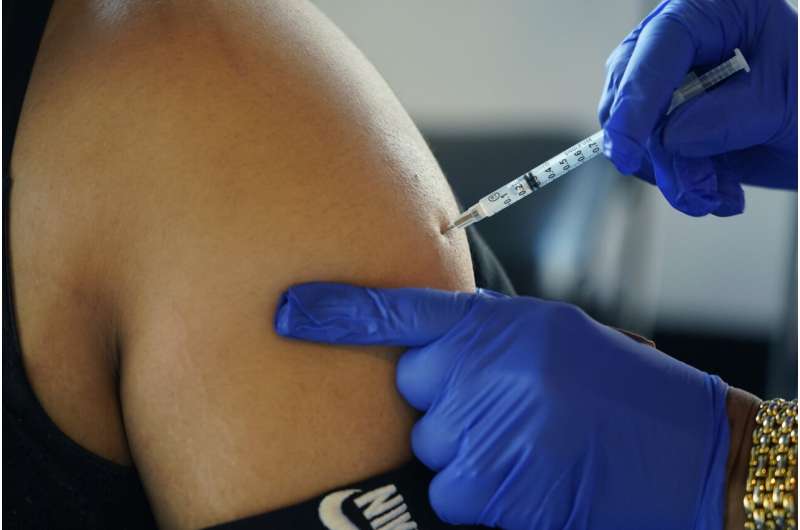
辉瑞和BioNTech已要求欧洲药品管理局授权其更新的冠状病毒增强疫苗,其中包括最新的omicron亚变种。
辉瑞在周五的一份声明中表示,它正在要求欧盟药品监管机构批准其COVID-19组合疫苗它的目标是原始冠状病毒和BA.4和BA.5, omicron的最新版本,目前全球绝大多数感染都是由这两种病毒引起的。辉瑞公司和BioNTech公司要求将疫苗提供给绿灯12岁以上禁止观看。
欧洲药品管理局(European Medicines Agency)目前正在审查是否批准Moderna和辉瑞公司(Pfizer)生产的针对BA.1亚型的升级版疫苗。BA.1亚型是该病毒的早期版本,现已被BA.4和BA.5取代;预计该决定将于下周做出。
辉瑞公司表示,如果这两种更新的COVID-19助推剂获得批准,其改造疫苗将“最早于9月”在欧洲上市。
上周,英国批准了Moderna针对BA.1版本omicron的更新版COVID-19增强剂,并表示将将其纳入该国的疫苗预防接种运动从下个月开始,50岁以上的人可以参加。
辉瑞和竞争对手Moderna本周都向美国监管机构提出了要求授权修改版本的加强疫苗注射,一半是原始配方,一半是BA.4和BA.5的保护。
卫生当局希望,经过调整的助推器可能会削弱今年冬天预期的COVID-19激增,但目前尚不清楚它们的效果如何。我们的赌注是,BA.5或类似的病毒今年冬天仍将传播,而接种这些最新疫苗仍将提供重要的保护。
进一步探索
©2022美联社。版权所有。未经允许,本材料不得出版、广播、重写或再分发。