科学家发现p38蛋白在心脏肥厚中的相反作用
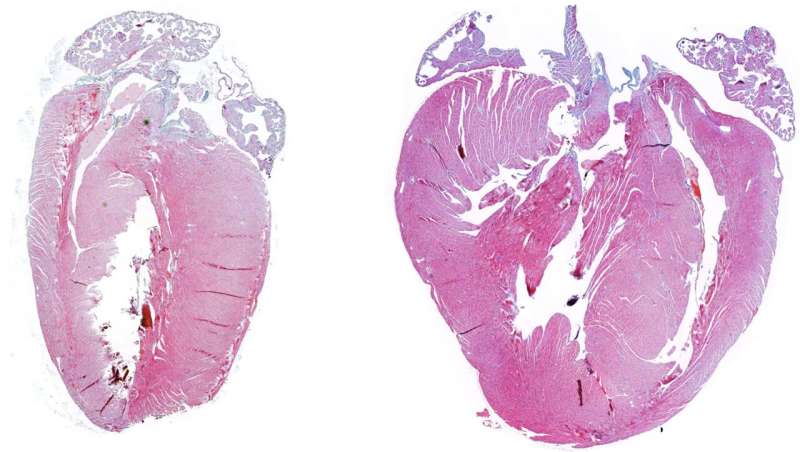
由Guadalupe Sabio博士领导的国家心血管研究中心(CNIC)的科学家进行的一项研究确定了MKK3/6-p38γ /δ信号通路在心脏肥厚发展中的关键作用。研究结果发表在该杂志上eLife,提示抑制p38γ/δ可能是肥厚性心肌病等疾病的有效治疗策略;然而,由于缺乏这些激酶酶的特异性抑制剂,这一途径仍未被探索。该研究还显示了抑制该蛋白家族的另一个成员p38α的相反效果,表明长期临床使用p38α抑制剂治疗慢性疾病有损害心脏的风险。
的人类的心脏每天跳动大约10万次,将血液泵到全身,为身体器官提供运转所需的氧气和营养物质。心脏不仅要在正常情况下满足对血液的需求,在压力条件下也是如此。为了达到这个目的,心脏有能力扩大大小,这个过程叫做肥大.第一作者拉斐尔·罗梅罗解释说,心脏肥大是出生后心脏生长的方式,也是体育锻炼的正常反应。但心脏肥大也可能由高血压和一些遗传疾病引发。
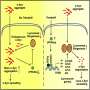
的收缩细胞心被称为心肌细胞的细胞包含许多分子通路,其激活促进心肌肥大。“其中之一就是p38通路罗梅罗解释说:“大脑皮层会对压力刺激做出反应。”p38蛋白控制着广泛的过程,它们的失调与许多疾病有关,使它们成为有希望的药理学靶点临床使用.然而,目前仅发现了一种p38亚型的特异性抑制剂,即p38α。正如Sabio博士所认识到的那样,“迄今为止的临床试验结果令人失望,但该途径的其他蛋白质,如p38γ、p38δ或上游激活剂MKK6,是有趣的可能的替代药理学靶点。”
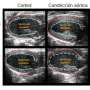
考虑到这一点,研究小组研究了抑制MKK6的安全性和潜在的长期负面影响。科学家们用基因改造过的缺乏MKK6的小鼠证明,缺乏这种蛋白质会降低预期寿命。这些小鼠在年轻时出现心脏肥大,随着年龄的增长出现心脏功能障碍。利用其他小鼠模型,研究人员发现,当MKK6缺失时,p38α的激活显著降低。
然而,p38α的失活促进了该途径的另一个分支的意外激活,包括蛋白MKK3, p38γ和p38δ。这种激活诱导了心脏肥厚发展的另一个关键途径,mTOR途径。
“我们已经确定了MKK3/6-p38γ /δ通路在疾病发展中的关键作用心脏肥大萨比奥博士说。“这意味着使用p38α抑制剂治疗慢性疾病,因为长期来看它们可能具有心脏毒性。与此同时,我们的研究结果表明,应该集中精力寻找可用于治疗心脏病的p38g和p38δ特异性抑制剂。”
进一步探索