破坏肿瘤细胞:使用注射材料的靶向免疫治疗
Terasaki生物医学创新研究所(TIBI)的研究人员开发并优化了一种微创方法,用于更有针对性、高效和持续地提供癌症免疫治疗。这种有针对性的方法减少了使用更系统的治疗方法时所经历的高剂量和可能的有害副作用。
身体的反应方式有很多种不正常的细胞或者外国入侵者。一种机制涉及到T细胞在免疫系统中,它们的表面有一种叫做"检查点的蛋白质“这些检查点蛋白与其他细胞表面的蛋白质结合,这可能导致刺激或抑制t细胞活性。”t细胞的刺激导致异常或入侵细胞的破坏,而抑制是一种内置机制,以防止免疫系统攻击人体自身的正常细胞。
然而,肿瘤细胞有时可以显示表面蛋白,这比肿瘤细胞免疫系统通过与t细胞结合并抑制它们的活性;这允许肿瘤细胞生长和扩散。近年来,“免疫检查点抑制剂”抗体(ICIs)被开发出来,它可以阻止肿瘤细胞与t细胞的结合。实际上,这会重新激活t细胞的免疫反应来破坏肿瘤细胞.在美国,ICIs已成功用于治疗肾脏、膀胱、肝脏和头部或颈部的癌症。
这些ICIs通常通过全身注射给药,尽管这些抗体已经证明了疗效,但其效果因患者而异。对于一些患者,这种输送的非特异性会导致过度的t细胞刺激,从而产生毒副作用。全身给药也会稀释ICI的有效性,需要更高的剂量和成本。
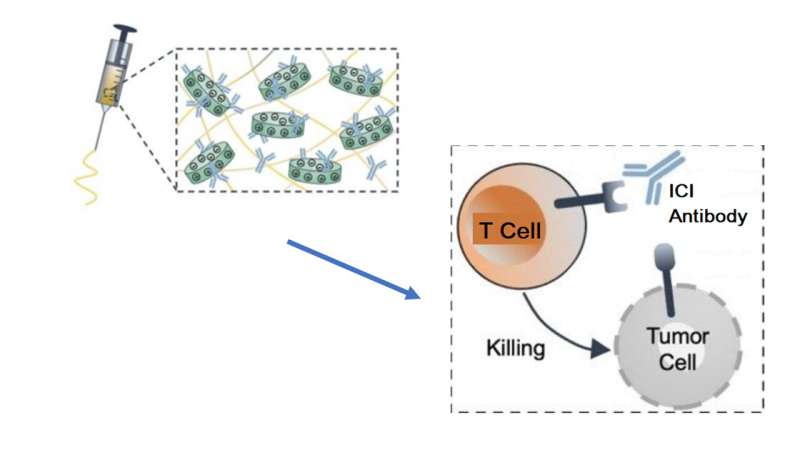
TIBI团队方法的主要特点是一种可注射的明胶生物材料,其中混合了盘状硅酸盐纳米片。纳米血小板含有带电表面,这是与ICIs保护性结合的最佳选择,同时使用微创注射将装载ici的生物材料运送到肿瘤部位。
明胶/纳米血小板混合物被优化为更有效的ICI输送和持续的药物释放。该团队还证明了几个因素,如纳米血小板、明胶和ICI浓度、pH值和生物材料降解条件,可以调节以控制特定肿瘤的ICI释放。
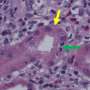
研究人员进行了额外的实验来测量他们的剪切减薄生物材料(STB)的功效,该材料在注射过程中会在压力下变形,并在注射后迅速自我恢复。这些STB被用于将ICIs注射到小鼠的黑色素瘤中。他们的研究结果表明,这些小鼠的黑色素瘤肿瘤生长速度最慢,尺寸最小,肿瘤和皮肤层之间的边缘清晰,没有炎症和炎症坏死组织;由于持续的ICI释放和传递,这些影响发生的程度要高得多,并且比阴性对照样本维持的时间更长。
由于ICI传递而激活的T细胞数量被量化,并且发现与阴性对照相比,带有stb传递的ICI的样本有超过44%的T辅助细胞和近36%的T杀伤细胞。
最后,研究肿瘤细胞的死亡情况。用不同染色技术进行的实验表明,在stb递送的样本中,肿瘤细胞死亡的数量是阴性对照样本的13.2倍。
“这里获得的结果清楚地证明了靶向、可控和可持续抗体的有效性交付以恢复人体对癌症的自然防御机制,”TIBI的董事兼首席执行官Ali Khademhosseini博士说。“它在创造联合疗法方面的潜力进一步扩大了其影响。”