研究人员推动CRISPR技术以前所未有的精度复制人类疾病
一种强大的新型基因组编辑技术使研究人员能够以前所未有的精度复制人类疾病,有望彻底改变一系列癌症的药物研发过程。
由WEHI团队开发的这项技术可以激活任何基因,包括那些被沉默的基因,从而允许新的基因产生药物在无可比拟的水平上探索耐药的目标和原因。
研究人员利用这种独特的技术首次复制了一种侵袭性淋巴瘤,他们用这种技术确定了一种基因,该基因导致了对澳大利亚目前使用的一种治疗血癌的新疗法的耐药性。
淋巴瘤是澳大利亚最常见的血癌,每年约有6500名澳大利亚人被诊断出淋巴瘤。双重打击淋巴瘤(DHL)是一种侵袭性亚型,影响称为B淋巴细胞或B细胞的白细胞。
该研究团队首次能够增强被称为CRISPR激活的基因组编辑技术,以准确模拟DHL。项目负责人Marco Herold教授说,该团队专注于DHL,因为这种疾病很难治疗,部分原因是缺乏有效的临床前建模。
“如果没有建模疾病的能力,在临床中正确测试哪些药物对其有效的机会就有限,”赫罗德教授说,他在WEHI建立并领导了澳大利亚最先进的CRISPR实验室之一。
“这项技术改变了游戏规则科学界以及诊所里的人们,因为它让我们能够模拟像DHL这样的疾病,并首次正确地测试针对它们的药物治疗。
“当你想到使用这个工具可以更好地模拟大量的人类疾病时,这就很重要了。”
这项研究引起了国际上的兴趣,WEHI团队与南京大学(中国)和罗氏集团成员基因泰克(美国)的研究人员密切合作,开发这项技术。
研究结果发表在自然通讯.
工程的阻力
Venetoclax 是WEHI与罗氏公司、基因泰克(罗氏集团成员)和艾伯维公司合作研究的结果,基于该研究所30多年来突破性的科学发现。它是由罗氏、基因泰克和艾伯维开发的。
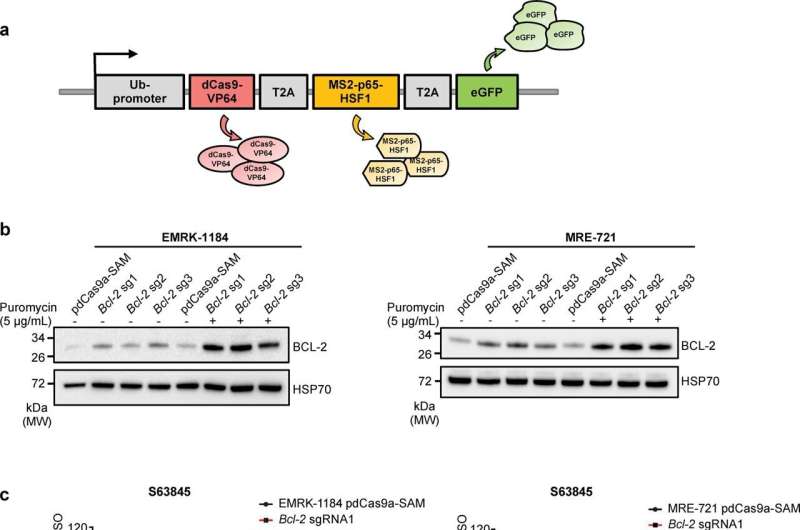
这种抗癌药物是基于WEHI在20世纪80年代末的一项发现,一种名为BCL-2的蛋白质可以帮助癌细胞无限期地存活。A1是BCL-2家族的促生存蛋白。该基因的激活在多种癌症中都有报道,包括白血病、淋巴瘤、黑色素瘤、胃癌和乳腺癌。
虽然A1一直被认为在癌症进展过程中起着重要作用,但博士生、第一作者邓叶轩(音)说,这一点直到现在还没有得到证实。邓说:“由于我们模型中的DHL淋巴瘤可以用venetoclax杀死,我们能够利用这一点首次证明A1是对这种药物耐药的主要因素。”
虽然癌症通常是通过打开基因来触发的,但研究人员在很大程度上只能在以前的疾病模型中关闭它们。项目负责人杰玛·凯利副教授说,他们的团队能够设计耐药性,因为他们的模型可以激活任何基因,甚至是那些被沉默的基因。
凯利副教授说:“我们利用这个模型前所未有的能力来打开A1,这使我们能够确认蛋白质是抗性驱动因素。”“我们的研究将允许更多的基因在其他模型中被激活,以更好地理解癌症重要的是,要确定驱动程序的其他原因耐药性."
三个“第一次”
联合第一作者Sarah Diepstraten博士说,这些发现表明A1是DHL有希望的药物靶点。
“之所以有这个发现,是因为我们能够为DHL创建一个模型,让我们可以打开任何基因,”迪普斯特拉滕博士说。“这证明了我们的技术在模拟人类疾病和探索药物靶标为什么有效或失败方面的力量,在无可比拟的水平上。”
这项研究,“生成一种CRISPR激活小鼠,使侵袭性淋巴瘤建模和venetoclax耐药性的询问成为可能”,发表在自然通讯.
进一步探索