细胞帮助免疫系统耐受友好的肠道细菌
威尔康奈尔医学院的研究人员领导的一项研究表明,被称为第3组先天淋巴样细胞(ILC3s)的免疫细胞在建立对人类胃肠道中共生微生物的耐受性方面发挥着重要作用。
该发现于9月7日报道自然,阐明了肠道健康和粘膜免疫的一个重要方面,这可能是更好的治疗方法的关键炎症性肠病(IBD)、结肠癌等慢性疾病。
“作为这项研究的一部分,我们定义了一种新的驱动途径免疫耐受胃肠道中的微生物群,”资深作者格雷戈里·f·索南伯格说,他是医学微生物学和免疫学副教授,消化病学和肝病科基础研究部门的负责人,也是吉尔罗伯茨炎症性肠病研究所和威尔康奈尔医学桑德拉和爱德华·梅耶癌症中心的成员。“这是我们对粘膜免疫理解的一个根本性进步,可能是理解当免疫过程中出现问题的关键免疫系统开始不恰当地攻击IBD等疾病中的微生物群。”
科学家们早就知道,数以万亿计的细菌、真菌和其他微生物共存于哺乳动物的肠道中。免疫系统通常是如何容忍这些“有益的”肠道微生物,而不是攻击它们的机制还没有得到很好的理解。但有证据表明,这种耐受性在IBD中被破坏,导致有害的肠道炎症发作。因此,对肠道免疫耐受的详细了解可能有助于开发针对ibd的强大新治疗方法,ibd是一类疾病,包括克罗恩病和溃疡性结肠炎,仅在美国就有数百万人患有这种疾病。
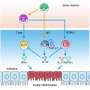
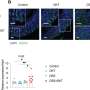
在这项研究中,Sonnenberg和他的同事,包括第一作者,Sonnenberg实验室的博士后研究员Mengze Lyu,使用单细胞测序和荧光成像技术来描绘免疫细胞在排出健康小鼠肠道的肠系膜淋巴结中。他们专注于表达转录因子RORγt的细胞,这种转录因子已知会在对肠道定植微生物的反应中驱动炎症或耐受性。他们发现,这些组织中主要的免疫细胞类型是T细胞和ilc3。后者是一组免疫细胞,是T细胞的天然对应物,在肠和肺等粘膜组织中起着第一道防线的作用。
通过与英国伯明翰大学的研究人员密切合作,科学家们观察到,在称为滤泡间带的淋巴结区域,ILC3s与一种特定类型的T细胞密切相关,称为rorr γ T +调节性T细胞(Tregs),其适应于降低炎症和免疫活动,以促进肠道的耐受性。
伯明翰大学免疫学和免疫治疗研究所的免疫调节教授David R. Withers说:“我们之前定义了ILC3s在调节适应性免疫中的关键作用,但这些发现令人兴奋,因为它们引发了一个概念,即ILC3s直接与Tregs相互作用,以控制肠道中的免疫耐受。”威瑟斯和他的实验室是这项研究的关键贡献者,也是索南伯格的长期合作者。
接下来,研究人员发现了ILC3s在促进肠道中RORγt+ Treg群体中发挥重要作用的证据。就像对致病微生物产生免疫反应一样,ILC3s呈现肠道微生物片段;但这引发了特异性识别这些微生物的RORγt+ treg,而不是炎症免疫反应。这些r γ T + treg然后抑制其他T细胞的反应,并加强对微生物群的耐受性。
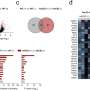
科学家们发现,当他们删除了ILC3s用来呈现微生物抗原的表面分子MHC II类,从而阻碍了ILC3s与RORγt+ Tregs的相互作用时,观察到的RORγt+ Tregs明显低于正常小鼠,受影响的小鼠出现了自发的肠道炎症。与此同时,炎症r γ T + T细胞,称为T辅助(Th)17细胞,在这些小鼠中显著增加,部分原因是许多treg,失去了来自ILC3辅助细胞的通常信号,变成了Th17细胞。
Lyu说:“我们广泛的研究表明,ilc3是对肠道微生物免疫耐受的必要和充分的执行者。”“此外,我们现在对ilc3用于与T细胞通信并驱动微生物群特异性treg生成的信号有了深入的了解。”
为了确认其与人类的潜在相关性,研究人员与临床儿科教授兼儿科消化病学部门主任robyn E. Sockolow博士密切合作,分析了儿童IBD患者或健康个体的炎症肠道组织样本。bob电竞威尔康奈尔医学院儿科的肝脏病学和营养学,纽约长老会科曼斯基儿童医院和高级消化护理中心的儿科胃bob电竞肠病学家。通过Socklolow和Roberts研究所活细胞库,他们发现了IBD患者ILC3s和RORγt+ Tregs之间的通信被中断的证据。
Sockolow说:“我们令人兴奋的结果为为什么IBD患者的免疫耐受性受损提供了一个潜在的解释,这可能会引发新的治疗方法,目的是重新教育免疫系统,以限制针对微生物群的慢性炎症。”
Sonnenberg和他的同事们现在正试图确定ILC3-T细胞耐受机制是如何区分共生有益微生物和致病微生物的。但迄今为止的结果表明,未来恢复ILC3功能的细胞疗法可能对抑制IBD炎症有强大的作用。此外,正如Sonnenberg实验室最近在多发性硬化症小鼠模型中所证明的那样,这种途径仍然有可能被利用来限制其他炎症和自身免疫疾病。
Sonnenberg指出:“ILC3s对于通过促进抗原特异性treg来协调耐受至关重要,这一事实尤其重要,因为它表明了高度靶向治疗的可能性,这种治疗可以精确地抑制不适当的免疫活动来源,而不损害整体免疫。”
进一步探索