深层蛋白质组学分析揭示成神经管细胞瘤可能的治疗靶点
根据发表在《美国医学杂志》上的一项新研究,深入研究在小鼠模型中生长的人类肿瘤的蛋白质和蛋白质活性,扩大了治疗成神经管细胞瘤的潜在治疗途径蛋白质组学研究杂志.
作为研究的一部分,希望之城(City of Hope)下属的转化基因组学研究所(TGen)、Sanford Burnham Prebys医学发现研究所和加州大学圣地亚哥分校(University of California, San Diego)的研究人员合作,从机制上解释了为什么药物放线菌素D可能是治疗3组成神经管细胞瘤的有用候选药物,这是基于先前药物筛选研究的发现。
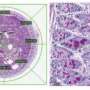
成神经管细胞瘤,小儿脑部最常见的恶性肿瘤肿瘤,有四个主要的分子亚型。3组肿瘤预后较差,5年生存率为50%。研究人员指出,对于所有成神经管细胞瘤,迫切需要更有效的治疗方法和毒副作用更小的治疗方法。
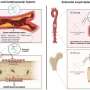
为了寻找新的治疗靶点,TGen博士后Kristin Leskoske博士和她的同事们研究了从20名不同亚型的髓母细胞瘤患者中提取的细胞在小鼠体内生长的肿瘤。产生的肿瘤称为原位患者源性异种移植或PDX模型。
“髓母细胞瘤的PDX模型是否足够接近原发性人类肿瘤的研究,在该领域存在一些争论药物测试Patrick Pirrotte博士说,他是TGen副教授,翻译质谱合作中心主任,也是该论文的高级作者。
他补充说,这项研究的一个重要结论是,“从蛋白质组学的角度来看,这些PDX肿瘤与实际患者的肿瘤非常相似,可以用作疾病的模型。”
该论文的第一作者莱斯科斯克博士说,直接在小鼠大脑中培养的细胞,而不是像有时那样在实验室培养皿中培养,或在小鼠侧翼植入,“更接近于模拟肿瘤正常生长的环境”。
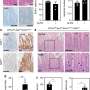
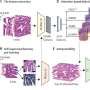
然后,研究人员深入分析了成神经管细胞瘤蛋白质组,测量了每个PDX模型中每种蛋白质的含量,并确定了蛋白质上的化学修饰,称为磷酸化,这表明了蛋白质的活性水平。
使用这些蛋白质莱斯科斯克博士及其同事能够将某些蛋白质的丰度或活性与其对特定药物的敏感性联系起来。例如,Sanford Burnham Prebys医学发现研究所的合著者Robert J. Wechsler-Reya博士先前的一项研究表明,3组成神经管细胞瘤对放线菌素D敏感,但这种敏感性的原因尚不清楚。
“药物筛选可以识别漏洞;他们不知道自己的作用机制。我们的补充蛋白质组学研究提出了放线菌素D敏感性的潜在机制,”Pirrotte博士说。
3组髓母细胞瘤最常见的分子特征是MYC扩增。在这项研究中,研究人员发现放线菌素D敏感性与MYC和MYC靶向基因丰度增加之间存在显著关联。
在这项研究中,许多对放线菌素D敏感的蛋白质是线粒体蛋白质,这是调节细胞代谢的关键。皮罗特博士说,该团队还有其他未发表的数据,结合这些发现,表明某些代谢缺陷可能是针对第3组肿瘤的。
MYC在其他癌症中也是一种众所周知的癌蛋白成神经管细胞瘤韦克斯勒-雷亚博士说。目前的研究结果应该鼓励我们寻找抑制这些myc驱动的癌症中线粒体功能的方法。”