2022年9月19日特征
耐药性是某些乳腺癌和卵巢癌的强大威胁。现在科学家正在弄清楚为什么
就像细菌一样,病毒和真菌制定了超特经抗菌药物的策略一样,癌细胞也可以对化学疗法具有抗药性。在肿瘤中,与三重阴性乳腺癌和卵巢肿瘤有关的肿瘤可以产生强大的抗性形式。
在一项有趣的研究方面,一个多中心的美国研究人员团队发现,乳腺癌和卵巢癌的表观遗传学特征最终可能指导医生的治疗决策,以众所周知,其癌症能够打破化学疗法的患者。
通过查明哪些分子特征与最佳治疗反应相关,肿瘤学家在设计治疗方案时可以更好地了解具有积极耐药性的声誉的癌症。
在报告科学翻译医学,康涅狄格州法明顿杰克逊基因组医学实验室的癌症生物学家阐明了为什么三重阴性乳腺癌(TNBC)和卵巢癌特别难以治疗。一方面,损失BRCA1或BRCA2基因活性在TNBC和卵巢癌中很常见科学家强调,并且对预后具有有效的影响。但是,涉及基因的改变的类型可能导致对治疗的反应不同。
与加利福尼亚州杜阿尔特市的华盛顿大学弗雷德·哈钦森癌症中心的医疗研究人员以及位于加利福尼亚州杜阿尔特的综合癌症中心的研究人员合作,科学家研究了涉及基因的各种缺陷如何影响对基于铂金化学疗法的反应。
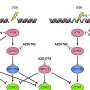
他们探索了涉及TNBC和卵巢癌的情况,其中有BRCA损失,基因改变以及被称为BRCA启动子甲基化的生物学现象。基因启动子甲基化是一种常见的表观遗传事件,发生在肿瘤发生过程的早期。甲基化是一个涉及原子转移的简单生化过程:一个碳和三种氢原子 - ch3- 从一个分子转移到另一个分子。科学家发现,甲基化具有诊断性和预后生物标志物的潜力。
“与BRCA1和BRCA2(BRCA2中的轴承突变)相比,用BRCA1启动子甲基化的三阴性乳腺癌和卵巢癌(BRCA1METH)对烷基化剂的回答效果更差,BRCA1和BRCA2(BRCA2) - 杰克逊(Jackson)研究的弗朗西斯卡·蒙希(Francesca Menghi)写道。第一作者。
基于铂的化学疗法是一种烷基化剂,一些TNBC或卵巢癌的妇女在接受这种形式的化学疗法治疗时表现不佳。孟希补充说:“这是一个难题,”他指出,她和她的团队通过对三重阴性乳腺癌和卵巢癌的详细基因组分析进行了解剖,并对患者衍生的异种移植物和基因工程细胞系进行了实验。结果不佳,”她强调。
TNBC是一种乳腺癌的一种形式,其中肿瘤细胞缺少三个关键受体:雌激素和孕激素受体缺失,人类表皮生长因子受体2(通常称为HER-2)也是如此。因此,术语,三重负。这些受体是用于成功治疗其他乳腺癌亚型的药物靶标,从而提高了患者的生存率。根据患者倡导组织,总部位于德克萨斯州达拉斯的苏珊·G·科门(Susan G.
由于尚未完全解释的原因,三阴性乳腺癌在年轻女性中最常发生,通常是40岁以下的年轻女性,尤其是黑人或西班牙裔。Menghi和她的同事在一项多管齐下的研究中发现,其BRCA基因中的突变患者也处于较高的风险中,并且患有BRCAMETH的人尤其面临不良预后的风险。
科学家长期以来知道三重负乳房和卵巢癌BRCA1和BRCA2基因中的突变可能对基于铂的化学疗法敏感。但是,由于顽固的原因,BRCA1中表观遗传启动子甲基化的癌症往往对以铂为中心的治疗的反应不太好。Menghi及其同事想知道为什么,并设计了一系列旨在取笑答案的优雅实验。
他们研究了人性化的小鼠模型,细胞系和遗传数据来自42例收到TNBC患者基于铂的化学疗法。研究人员比较了BRCA的表观遗传和遗传变化(促促甲基化或BRCA1的遗传丧失)如何影响患者和小鼠对基于铂基化疗的反应。尽管两种亚型都导致了类似的下游遗传特征,但BRCA1启动子甲基化急剧地赋予了具有铂 - 疗法耐药性的肿瘤,并与较差的结果有关。
“我们发现,尽管与BRCA1METH和BRCAMUT状态相关的下游基因组突变特征相同,但BRCA1METH统一地与结果相关,” Menghi及其同事报道说。科学翻译医学。
“接触Brca1meth三重阴性乳腺癌对铂化学疗法的暴露,无论是对患者的临床治疗还是作为临床前患者衍生异种移植物的体内暴露的实验性治疗,导致BRCA1甲基化的等位基因丧失,并增加了BRCA1表达和铂抗性,”。
团队得出的结论是,他们的数据回答了有关Brcamut和Brcameth的一些关键问题:该团队说,Brcamut Cancers是一种基因“固定”的缺陷状态。另一个子类型是一个完全不同的故事。BRCA1METH癌症对基因毒素的暴露高度适应,并且由于促进剂甲基化,对治疗具有抗药性。
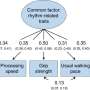
孟吉总结说:“我们进一步发现,与增强对铂化化疗的反应相关的特定增强免疫转录信号,但仅在BRCA癌症患者中。”“在TNBC和[卵巢癌]可能被我们的决策树确定会对癌症幸存者产生有意义的影响。”
进一步探索
©2022科学BOB体育赌博X网络