断裂的基因组,阿尔茨海默氏症神经元打电话求助
Picower研究所的研究人员的一项新研究在麻省理工学院学习与记忆提供了证据来自小鼠模型和后期人体组织之间的直接联系的两个问题出现在阿尔茨海默氏症:一个累积的DNA双链断裂(双边带)神经元和小胶质细胞的炎症性行为,大脑的免疫细胞。
一个关键的新发现神经元主动触发一个炎症反应他们的基因损伤。神经元没有大脑的信号免疫系统在阿尔茨海默病,研究作者格温妮丝•韦尔奇说,前麻省理工学院大脑与认知科学系研究生在实验室的资深作者Li-Huei蔡。
在神经科学:“这是一个小说概念的想法,神经元可以在应对DNA损伤激活炎症活动,”韦尔奇说。“一般的想法是,神经元更被动与小胶质细胞对与年龄有关的神经炎症的关系。”
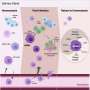
相反,韦尔奇,蔡,报告的合著者科学的进步是神经元应对越来越多的双边带经过第一阶段试图修复断裂的DNA,然后当它显然失败了,小胶质细胞发送通过分子信号,作为回应,承担更多的炎症状态。在实验中,科学家们打断了免疫信号,他们阻止小胶质细胞进入状态和有辱人格的神经回路连接,或突触。
蔡的实验室的成员研究双边带在十多年的阿尔茨海默氏症。蔡说,新发现增加了新兴的理解在阿尔茨海默氏症中扮演重要角色。
“我们有一个长期的兴趣了解神经元DNA断裂,“蔡说,Picower神经科学教授和麻省理工学院的创始人老化的大脑活动。“我们先前表明,DNA双链断裂是必要的感应activity-regulated神经元基因表达,但我们也观察到的DNA损伤神经元在神经退行性病变的早期阶段。
“我们现在知道,在引发DNA-damaged神经元发挥积极的作用免疫反应蔡说:“也许小胶质细胞和星形胶质细胞。“这是由NFkappaB转录因子的激活。此外,我们确定了两个细胞因子分泌受损神经元招募小胶质细胞,引起小胶质反应。重要的是,我们表明,抑制NFkappaB获救突触神经退化损失,进一步阐明神经免疫反应对突触完整性和认知功能的影响。”
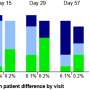
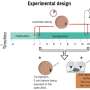
在她的论文研究韦尔奇使用实验室的“CK-p25“阿尔茨海默氏症的小鼠模型,可以诱导疾病病理学,她注意到一个神经元的时间表与双边带出现在一周内,在两周后数量达到高峰,然后逐渐减少,变得明显减少了六个星期。与此同时,这些神经元也失去了他们的表达能力的标准标记神经元的身份。韦尔奇意识到似乎有阶段应对双边带的过程。第一个神经元有一些双边带和强烈的身份(基线),然后高双边带的身份(阶段1),然后高双边带和神经元身份丢失(阶段2)。
成绩单告诉故事
了解细胞在每个阶段做不同,韦尔奇和团队使用多个“转录组”技术,追踪基因表达的差异。她的分析显示,神经元在基线标识基因表达最强烈,DNA修复基因强大的第一阶段期间,和免疫信号传导基因在第二阶段尤为突出。
在免疫信号传导基因的由主转录监管机构NFkappaB。这些包括细胞因子Ccl2, Cxcl10。
看看这些变化是由于具体双边带,韦尔奇治疗没有任何诱导的神经元病理导致双边带和一个叫依托泊苷的化学。类似的基因表达模式明显诱导小鼠在依托泊苷处理的完成。当韦尔奇也看着基因表达在人与双边带和阿尔茨海默氏症的大脑她还发现许多重要的重叠。
“我们发现阶段1和阶段2基因签名是活跃在人类DSB-bearing神经元,“她和她的合著者写道。“这神经免疫签名的上下文中被进一步放大广告病理学,这表明它可能在疾病有关的神经炎症服务功能的作用。”
小胶质细胞的重要角色
建立DSB-afflicted神经元采用NFkappaB发出免疫信号如Ccl2和Cxcl10,韦尔奇和团队接着问效果是什么。考虑到实验室2017年特点一个晚期炎症反应的小胶质细胞在阿尔茨海默氏症,他们假设神经元可能是负责任的。
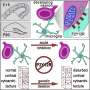
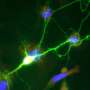
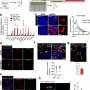
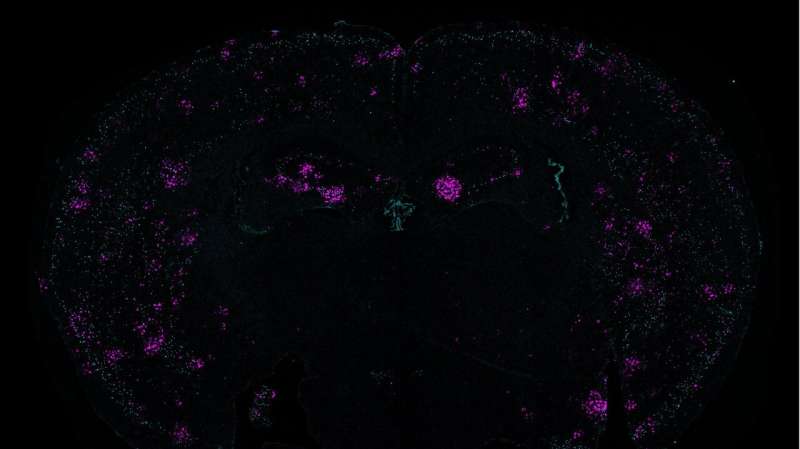
韦尔奇使用空间转录组分析。她uninduced和诱导小鼠的大脑分成许多地区,和额定每个区域根据他们的双边带信号的强度。然后她分析基因转录在每个区域,发现高双边带的位置也有更多的小胶质细胞在炎症状态比双边带较低的位置。他们也可以直接形象的关系,产生炎症的观察小胶质细胞(显示异常大的细胞体)共存与high-DSB神经元。
进一步测试的假设,他们中断NFkappaB转录调节神经元通过干扰的关键分子齿轮机械称为p65。这一步导致减少扩散小胶质细胞和小胶质细胞胞体大小。它还引发有益的小胶质细胞的变化基因表达,使他们更符合正常的“稳态”状态。
在其他实验中他们发现etoposide-treated神经元表达Cxcl10和Ccl2但扰乱NFkappaB表达减少。他们也看到,消耗的两个分子的大脑也阻止小胶质细胞成为活性。
回顾神经元,他们看到,尽管推倒NFkappaB活动没有阻止他们死亡,它保护电路连接,或在神经元突触,仍然活着。这很重要,因为这些电路连接构成大脑功能和小胶质细胞被修剪。
因为众所周知NFkappaB有助于防止细胞死亡(这可能就是为什么敲下来没有阻止神经元死亡),韦尔奇说敲下来不可能是一个治疗的策略。
”其证明的原则,如果你关掉的主要开关炎症,这将改变小神经胶质细胞和神经元相互作用,”她说。“如果你的目标是目标炎症通路,专注于特定的信号分子可能更精确的方式进行干预。”
除了韦尔奇和蔡,论文的其他作者Carles Boix,以罗伊Schmauch, Jose Davila-Velderrain Matheus维克多,毗瑟奴Dileep, p .洛伦佐Bozzelli俏苏,Jemmie d . Cheng Audrey Lee诺艾尔Leary,安德烈亚斯·r·Pfenning, Manolis >。
更多信息:格温妮丝•韦尔奇et al,神经元受到DNA双链断裂引起小胶质细胞激活通过antiviral-like信号在神经退化。科学的进步(2022)。DOI: 10.1126 / sciadv.abo4662。www.science.org/doi/10.1126/sciadv.abo4662