炎症、衰老和饮食有什么关系?首次描述了系统的监管网络
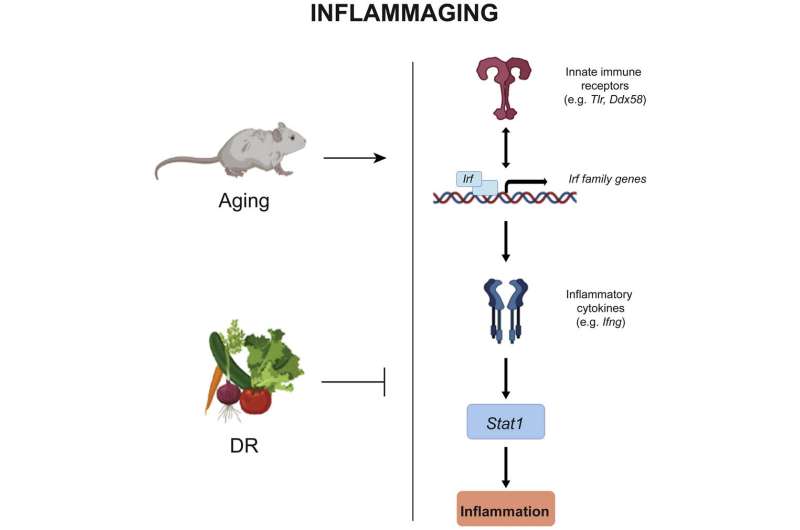
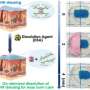
组织中轻度、持续的炎症被认为是人类衰老过程的生物学标志之一,同时也是阿尔茨海默病或癌症等疾病的风险因素。耶拿莱布尼茨衰老研究所-弗里茨利普曼研究所(FLI)的Francesco Neri教授和Mahdi Rasa博士首次成功地在分子水平上描述了驱动一般多器官炎症反应的调节网络。此外,他们能够证明饮食限制可以影响这一调节回路,从而抑制炎症。
炎症是身体的一种免疫反应,它本身是有用的:我们的免疫系统用它来对抗病原体或从组织中移除受损细胞。一旦免疫细胞完成了它们的工作,炎症就消退了:感染结束了,伤口也愈合了。不像这种急性炎症,与年龄有关慢性炎症不是本地的。的先天免疫系统增强其整体活性,导致慢性低度炎症。这种与衰老相关的炎症也被称为炎症。
炎症损害健康
这种潜在的炎症对健康有影响。“如果你有一个恒定的激活免疫细胞这可能会导致它们精疲力竭,当你感染时,这反过来又会导致问题。免疫细胞可能不再正常反应。炎症也与癌症的发展有关,因为在炎症组织中,我们看到细胞增殖增加,”Francesco Neri教授解释说,他在耶拿的莱布尼茨衰老研究所-弗里茨李普曼研究所(FLI)领导“衰老的表观遗传学”研究小组,直到2021年底。这位生物学家目前在意大利都灵大学教学和从事研究。
衰老、炎症和饮食是如何相互作用的?
Neri教授与Mahdi Rasa博士和FLI的其他同事一起,在小鼠身上进行了一项研究,以调查伴随衰老的慢性炎症是如何被基因调节和维持的,以及饮食限制是否能影响这一调节网络并抑制炎症。事实上,过去20年的研究表明,各种动物——从苍蝇到蠕虫,从啮齿动物到猴子——在喂食减少脂肪含量的食物时,寿命更长热量摄取.
例如,当老鼠少吃30%的食物时,它们更健康、更活跃,寿命延长了三到四个月——相当于寿命增加了10%到15%。在限制卡路里饮食的人群中,健康状况也有所改善。众所周知,这种饮食方法可以减少炎症反应。然而,炎症、衰老和饮食限制都有详细规定分子水平上,以及它们之间的关系,目前还不清楚。
炎症反馈回路
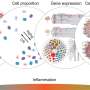
他们目前的研究最近发表在杂志上细胞的报道, FLI的研究人员首先比较了4个月大的小鼠和年长的小鼠(22个月大)。与之前的研究相反,基因的活性不仅在一个器官中测量,而且在多个平行组织中测量:血液、大脑、心脏、肾脏、肝脏、肺、肌肉和皮肤。
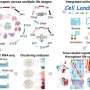
Neri解释说:“我们的首要任务是研究所有组织中受影响的通路,以便在系统水平上了解炎症。”“我们发现,老年小鼠炎症阶段的特征是一组编码先天免疫系统受体的特定基因的上调。这种上调导致一组干扰素调节基因的激活。这些基因激活其他产生炎症细胞因子的基因,同时激活Stat1,这是一个主要的转录因子,用于调节基因与炎症有关。整个过程就像一个正反馈循环,让炎症状态持续下去。”耶拿的研究人员因此是第一个描述跨器官和系统调节网络的人。但是,减少卡路里摄入能打断这个循环吗?
为了回答这个问题,Neri和Rasa研究了另外两组啮齿动物器官中的基因活动:一组小鼠几乎一生(4到22个月)都被少给了30%的食物,另一组小鼠在生命结束时只在这种条件下呆了两个月。无论热量限制是短期的还是长期的,总的来说,这种饮食对研究的所有器官都有积极的影响,除了心脏。
系统的监管网络是干预的起点
通过他们的工作,这两位研究人员也为未来与衰老相关的慢性疾病的药物治疗提供了起点炎症.“在这监管网络例如,TLR4是一种编码先天免疫系统受体的基因,”Rasa博士解释道,他将基因分析作为博士论文的一部分。“受体就像一个SOS信号,当没有病原体需要对抗时,我们就不需要它了。如果我们能下调TLR4,我们就能减少衰老过程中的慢性炎症反应。”
另一种被广泛讨论的干预可能性是服用维生素或益生菌等膳食补充剂,目的是影响消化道微生物的组成。“饮食限制似乎可以改变微生物群,从而减少炎症。如果有可能通过膳食补充剂来改变肠道微生物群,那么在不需要限制饮食的情况下也可以达到同样的有益效果。”内里教授承认,这仍然只是猜测。“我们首先需要更好地理解其中的过程。”
进一步探索