潜在目标绕过黑色素瘤治疗抵抗免疫检查点阻滞剂
在过去的十年里,免疫阻断剂检查站,或者银行独立委员会,已经彻底改变了各种先进的癌症治疗,包括黑色素瘤、最激进的皮肤癌,不久前很大程度上被认为是无法治愈的。然而,四分之三的对银行独立委员会的晚期黑色素瘤患者的抵抗力。
现在,在发表的一份报告自然通讯,研究人员揭示潜在的采用批准的临床药物ruxolitinib——抑制ICB-resistant黑色素瘤。
“由于ruxolitinib临床批准,并在患者进行了测试先进的实体肿瘤,非小细胞肺癌和三阴性乳腺癌,我们的研究证明患者ruxolitinib先进的进一步测试黑素瘤对银行独立委员会,”Lewis Zhichang Shi说,医学博士,Ph.D., an associate professor in the University of Alabama at Birmingham Department of Radiation Oncology.
史指出ruxolitinib可能需要结合其它治疗方法达到一个长期的治疗。
六年来,知道肿瘤失去移行细胞信号是两个银行独立委员会药物抵抗的主要机制,anti-CTLA-4 anti-PD-1。然而,如何克服这种阻力仍然难以捉摸。
这种损失的移行细胞信号在人类黑色素瘤是由移行细胞信号通路中的基因的失调。然而,在小鼠模型可拆卸的突变未能显示亏损移行细胞肿瘤细胞信号调制肿瘤浸润T细胞的活动,或尖,因为这些模型还包含一些移行细胞信号。直到免疫细胞癌症控制是至关重要的,因为它们能够探测和摧毁肿瘤。然而,在对抗手段,癌症学会逃避这种破坏通过提高免疫检查站他们细胞表面的蛋白质,这些蛋白质表面尖发送一个“关闭”信号。
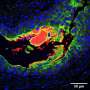
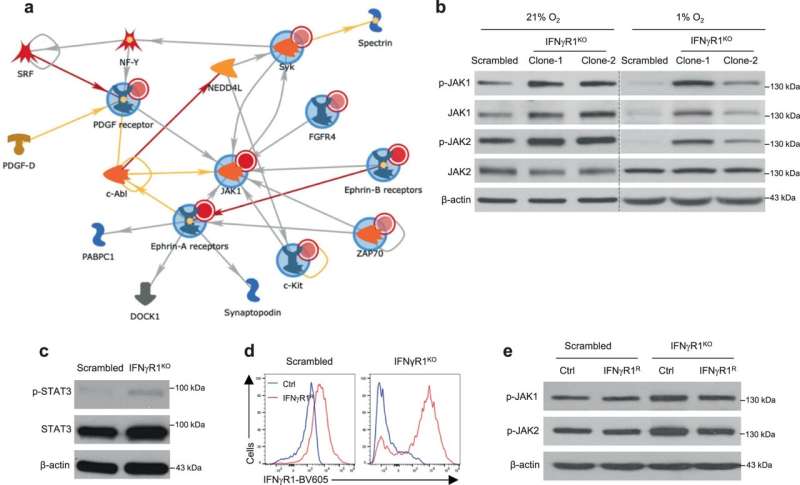
所以研究人员由史和UAB放射肿瘤学部门主席詹姆斯·a·邦纳医学博士,created a cleaner mouse melanoma model by knocking out the receptor gene for interferon-gamma signaling. They used this improved knockout model—called IFNγR1KO—to probe the mechanisms of ICB resistance and how the IFNγR1KO melanomas alter the response of TILs to ICBs.
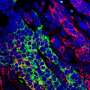
non-knockout黑色素瘤相比,鼠标IFNγR1KO黑色素瘤显示减少渗透等尖CD8杀手T细胞,和尖降低了对肿瘤免疫活动。这表明正常的黑色素瘤移行细胞信号传导中发挥着重要作用塑造尖。以证实这些临床前研究结果,研究人员,合作则臣Chong,博士,助理教授UAB的遗传学和信息学研究所也做了生物信息学分析人类黑色素瘤的癌症基因组图谱的数据。他们发现黑色素瘤与减毒移行细胞信号也有签名T细胞基因的表达减少,表明T细胞浸润减少和功能。
机械化,IFNγR1KO小鼠黑色素瘤的网络不断活跃JAK1/2激酶激活蛋白酪氨酸激酶为中心,这种细胞内信号通路被激活介导mTOR信号。
Ruxolitinib JAK1/2抑制剂。研究人员发现ruxolitinib IFNγR1KO黑色素瘤抑制癌细胞的增长,但不是控制黑色素瘤。实验的T细胞耗竭或主机肿瘤坏死因子信号完全废除ruxolitinib功效,主要研究人员得出ruxolitinib IFNγR1KO黑色素瘤的抑制取决于T细胞和宿主细胞因子肿瘤坏死因子。研究人员还发现,ruxolitinib介导重组的尖的治疗效果,而不是通过直接杀死肿瘤细胞。
史和邦纳说他们现在正在积极征求临床兴趣探索JAK1/2抑制策略绕过银行独立委员会抵抗黑色素瘤患者,一个紧迫的尚未被满足的医疗需求。
Co-first研究的作者,“选择性抑制黑素瘤缺乏IFN-γ通路的木菠萝抑制取决于T细胞和宿主TNF信号,“红星沈,在实验室,博士后学者和博士生Fengyuan黄庄组。
进一步探索