研究团队创造更有效的淋巴癌疗法
淋巴结转移是癌症患者病情恶化的标志,及时治疗至关重要。
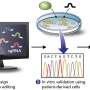
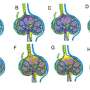
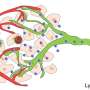
来自东北大学生物医学工程研究生院的一个研究团队开发了一种淋巴药物输送系统(LDDS),其中抗癌药物直接注射到转移的LNs中。当联合全身照射(TBI)时,新型LDDS对早期淋巴结转移的抗肿瘤效果优于常规化疗。
TBI向全身提供均匀剂量的辐射,穿透传统化疗无法到达的区域。近年来,外伤性脑损伤在激活免疫反应和改变免疫功能方面显示出积极的结果肿瘤微环境.同时LDDS主要用于局部转移性LNs的治疗。
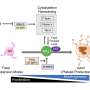
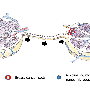
该研究小组希望扩大LDDS的使用范围,以防止远处转移——即癌症从基底细胞扩散原发肿瘤到远处的淋巴结。研究生Shota Sora说:“我们知道,增强全身肿瘤免疫效果的联合治疗将是一种重要的治疗策略。”他是Tetsuya Kodama教授领导的研究团队的一员。
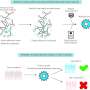
Sora和他的同事在转移模型小鼠上研究了LDDS和TBI对LN和远处转移的双重治疗。他们使用辐照伽马射线(一次性剂量为1.0 GY)和用溶剂调节的抗癌药物CDDP,使其渗透压为1987千帕,粘度为11.3 mPas。
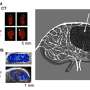
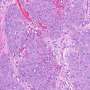
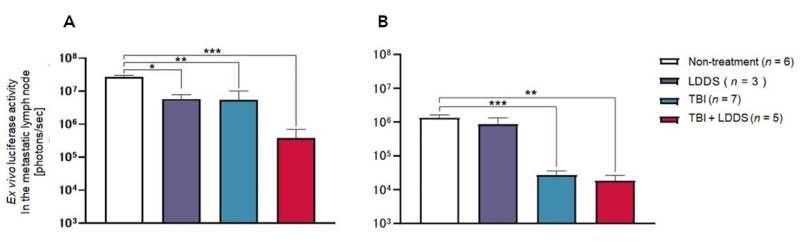
体内生物发光成像系统,高频超声系统,和组织学显示新疗法比单独使用LDDS或TBI更有效。治疗后,脾脏中免疫反应相关基因(CD4、CD8和IL-12b)的表达增加,表明免疫反应被激活。
“结果表明TBI和LDDS都能提高LB转移和远处转移的治疗效果,这种新方法是一种有前途的治疗方法癌症患者苍井空补充道。
他们的研究细节发表在杂志上癌症科学2022年9月9日。
进一步探索