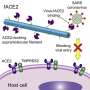
一种抗癌药物如何被重新利用来对抗导致疟疾的寄生虫
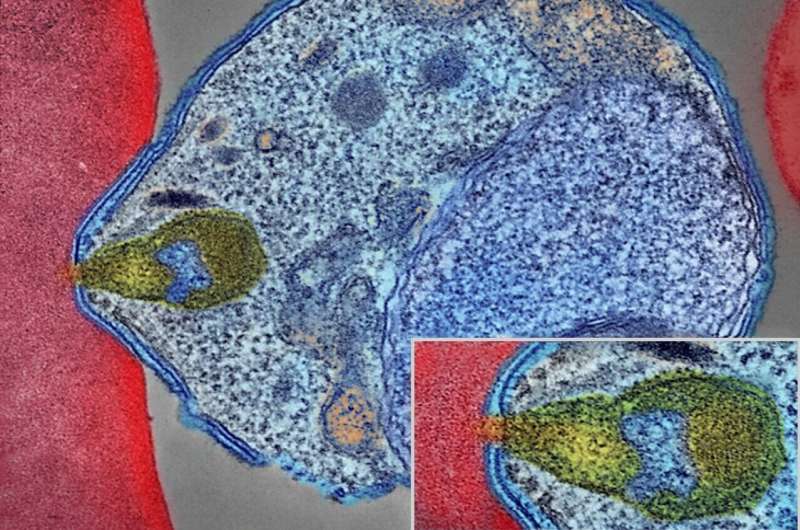
疟疾是由由蚊子传播的恶性疟原虫引起的。世界卫生组织(世卫组织)估计,2020年有全世界有2.41亿例病例和62.7万人死亡在美国,94%的病例和96%的死亡发生在撒哈拉以南非洲。不幸的是,每分钟都有一名五岁以下儿童死于疟疾。
随着蚊子栖息地的扩大全球变暖,人们更容易感染疟疾寄生虫.世界卫生组织建议病媒控制减少蚊子的数量,从而减少蚊子叮咬的可能性,以及化学预防在缺乏有效疫苗的情况下预防疾病。
弓形虫是疟原虫的近亲,全世界有20亿人感染,是这种食源性疾病的病因弓形体病.婴儿和免疫系统受损的人,如艾滋病或癌症患者,更容易感染这种疾病。研究还表明,弓形虫寄生虫长期影响一个人的性格和行为取决于自己的能力所窝人类的大脑它们可能在精神分裂症和躁郁症中发挥作用。
尽管科学家们为根除这两种寄生虫传播的疾病做出了不懈的努力,但目前可用来治疗它们的药物并不理想,而且几乎没有替代品。
不良副作用
弓形虫病的治疗通常有严重的副作用例如肝毒性和骨髓抑制,骨髓参与血细胞的产生,使免疫功能低下的人面临更大的风险。此外,当弓形虫在肌肉和大脑中形成潜伏感染时,没有药物可以杀死弓形虫。即使药物确实存在,成本也可能是一个因素——2015年,达拉匹林(Daraprim)成为了新闻图灵制药公司将价格从每片13.50美元提高到750美元在美国,这威胁到弱势患者的就医机会。
在疟疾流行的地方,以青蒿素为基础的联合疗法(ACTs)现在是一线治疗方法。青蒿素是一种植物提取物,起源于传统的中草药疗法,最早由科学家合成屠呦呦博士他获得了2015年诺贝尔奖。然而,一个主要的担忧是对青蒿素和替代药物的耐药性的蔓延药物组合,最初在东南亚最近在卢旺达和乌干达.当一种药物失去效力,不能再完全治愈它原本要治疗的感染时,就会出现耐药性。
一种可以节省大量时间和金钱的药物开发策略“重新利用”治疗方法最初被批准用于其他疾病或状况。一个著名的例子是西地那非,最初开发用于治疗冠状动脉疾病引起的胸痛。虽然它失败了临床试验,科学家们发现这种药物的副作用之一是勃起,它的目的是伟哥该公司治疗勃起功能障碍。研究人员竞相开发COVID-19疗法在美国,药物再利用受到了广泛关注。
用一种新药对抗寄生虫
我们的团队刚刚取得了科学突破,发现了一种抗寄生虫的新药,altiratinib.最初是为了治疗胶质母细胞瘤阿替替尼是一种侵袭性脑癌,我们确定阿替替尼对弓形虫有很强的杀寄生活性。Altiratinib对艾美耳菌和新孢子菌也有效,这两种寄生虫具有重要的兽医意义,会给牲畜造成重大经济损失。
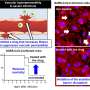
在讨论药物时,科学家们经常使用这个术语“作用机制”(MOA)来描述药物在人体内的实际作用。为了更好地理解阿替替尼如何在寄生虫中起作用,确定它的“目标”是圣杯。利用尖端遗传学,我们确定了altiratinib的主要目标是一种激酶——一种化学修饰其他分子并调节其生物活性的酶。在弓形虫中,这种激酶被称为PRP4K,而在疟原虫中,它被称为CLK3。
大多数细胞功能是由蛋白质完成的,蛋白质是一种复杂的大分子。允许细胞制造蛋白质的信息包含在DNA中。特定蛋白质的生产开始于相应基因的转录(即“复制”)到未成熟的信使RNA分子(mRNA)。
未成熟的mRNA是一项“正在进行的工作”,类似于需要打磨的粗略草图。在第二步中,mRNA将经历一个名为“剪接”的过程。酶会去除未成熟的mRNA分子中不必要的部分,就像裁缝修饰一件衣服一样。由此产生的“成熟”mRNA可以被视为用于蛋白质生产的“最终草图”。如果在剪接过程中出现问题,产生的蛋白质可能无法正常工作,或者根本无法工作。
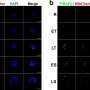
激酶PRP4K是参与这一剪接步骤的“裁缝”之一。altiratinib对其的抑制在全基因组水平上破坏了寄生虫的剪接,导致蛋白质生产混乱和寄生虫死亡。
确定感兴趣的区域
蛋白质的某些区域与环境中的分子相互作用,因此对其功能至关重要。使用最先进的方法,我们能够确定PRP4K的区域化学反应发生并与阿替替尼结合。如果结合位点定义更明确,就能制造出更有效的化合物。
我们还了解到更多关于多物种抗疟疾药物的信息tcmdc - 135051,即尚未上市.它也可以结合PRPK4,而且由于TCMDC-135051和altiratinib具有如此不同的化学空间,并且可能以不同的方式起作用,因此可以基于两者的组合开发治疗方法,这在理论上可以限制耐药性的发生。
我们的发现突出了PRP4K/CLK3激酶作为寄生虫药物靶点的重要性,并使最初用于癌症治疗的altiratinib不仅成为治疗疟疾的一种治疗选择,而且还可以用于治疗弓形虫病和寄生虫易发动物疾病。