在新的大脑模型中,COVID-19与神经细胞之间的连接过度破坏有关
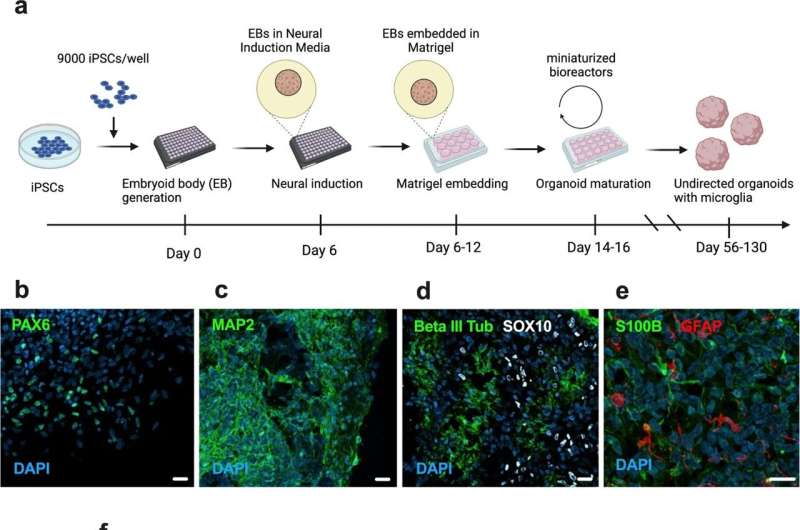
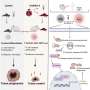
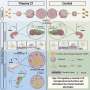
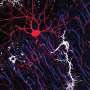
卡罗林斯卡学院的研究人员在一项新研究中使用细胞重编程创建了人类三维大脑模型,并用SARS-CoV-2感染这些模型。在受感染的模型中,大脑免疫细胞过度消除突触,并获得了一种模仿神经退行性疾病中观察到的基因表达模式。这一发现可能有助于确定针对COVID-19感染后持续认知症状的新疗法。
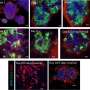
多项研究报告了COVID-19感染后持续的认知症状,但其潜在机制尚不清楚。这项研究的研究人员发表在《即时通讯》杂志上《分子精神病学》他们从人类诱导多能干细胞(iPS)中创建了大脑的三维模型——所谓的脑类器官。该模型与之前的类器官模型不同,因为研究人员还包括了大脑免疫细胞- - - - - -小神经胶质细胞在模型中。
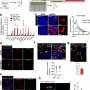
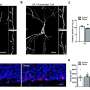
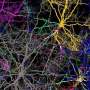
在感染模型中,小胶质细胞过度吞噬突触结构,并表现出吞噬作用相关因子的上调。开发的模型和研究结果可能有助于指导未来针对COVID-19和其他神经侵入性病毒感染后的认知症状的努力。
感染后的认知障碍
“有趣的是,我们的结果在很大程度上模仿了最近在感染其他神经侵入性RNA病毒(如西尼罗河病毒)的小鼠模型中观察到的结果。这些病毒还与感染后残留的认知缺陷有关,小胶质细胞的持续激活导致突触过度吞噬,这被认为是导致这些症状的原因。多项研究现在还报告了COVID-19感染后剩余的认知症状,以及被诊断为以认知症状为特征的疾病的风险增加,”该研究的共同第一作者Samudyata说,他是卡罗林斯卡学院生理学和药理学学系Sellgren实验室的博士后。
与帕金森和阿尔茨海默病有关
小胶质细胞是大脑的常驻免疫细胞,但在发育和成人中也执行重要的神经元回路调节功能大脑.其中一个重要功能是吞噬多余的突触,这一过程被认为可以改善和维持认知功能。然而,突触的过度吞噬与神经发育障碍,如精神分裂症,以及包括阿尔茨海默病在内的神经退行性疾病有关。
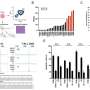
通过测序单个细胞,作者还可以研究模型中不同类型的细胞对病毒的反应。
“小胶质细胞显示出一种独特的基因特征,其主要特征是干扰素反应基因的上调,包括先前与帕金森病和阿尔茨海默病等神经退行性疾病有关的途径。该研究的合著者、卡罗林斯卡学院生理学和药理学系Sellgren实验室的博士生Susmita Malwade说:“在病毒载量最低的稍后时间点也观察到了这一特征。”
研究人员现在将研究不同的药理学方法如何逆转感染模型中观察到的变化。