新策略显示在神经退行性疾病中阻断神经损失的潜力
圣路易斯华盛顿大学医学院(Washington University School of Medicine)的两项新研究支持开发一种广泛适用于神经退行性疾病的治疗方法,该方法针对的是一种分子,它在神经系统的线路轴突死亡过程中起着中央刽子手的作用。
阻断这种分子刽子手可以防止轴突丢失,这与许多神经退行性疾病有关周围神经病变帕金森病和青光眼肌萎缩性脊髓侧索硬化症(肌萎缩性侧索硬化症)。
这两项新研究都发表在10月26日的《美国科学》杂志上临床调查杂志,揭示了被称为sarm1的分子如何触发神经退行性疾病发展的基础轴突死亡的惊人细节。该研究还指出了以轴突丢失为特征的疾病的新治疗方法。
“我们迫切需要神经退行性疾病的治疗方法,”共同资深作者杰弗里·米尔布兰特说,他是医学博士、博士、詹姆斯·s·麦克唐纳教授和遗传学系主任。“有了SARM1在这些疾病中的中心作用的证据,我们非常有兴趣找到阻断这种分子的方法——无论是小分子抑制剂还是基因治疗技术。我们最新的研究表明,我们也可以干扰它驱动破坏性神经炎症的能力。我们希望这项工作将为一系列神经退行性和神经炎症疾病带来有效的新疗法。”
2017年,Milbrandt和共同资深作者Aaron DiAntonio,医学博士,发育生物学Alan A.和Edith L. Wolff教授发现,SARM1是一种可以促进神经退行性变的酶。不久之后,他们共同创立了一家创业公司名为缴械疗法,以促进抑制SARM1的药物化合物的开发,用于治疗以轴突变性为特征的疾病。2020年,裁军治疗公司被礼来公司收购,以进一步开发针对神经退行性疾病的sarm1靶向疗法。
在健康的神经元中,SARM1总是处于关闭状态。但在受伤或疾病后,SARM1会变得活跃。激活的SARM1是一个纵火犯,它燃烧了如此多的细胞能量,以至于轴突无法存活。这能源危机触发轴突分解。
为了进一步了解SARM1在触发轴突破坏中的作用,研究人员研究了一种神秘且极其罕见的进行性神经病变综合征——罕见到连名字都没有。这罕见的疾病这是一个很好的模型用来理解免疫系统在神经炎症条件下的作用。对患者基因组进行测序后,研究人员发现轴突丢失是由基因中的遗传错误引起的NMNAT2它的正常功能使SARM1处于关闭状态。由于这些基因错误,SARM1不断被激活,触发轴突破坏。研究人员使用CRISPR基因编辑技术在老鼠身上重现了这些突变。和患有该综合症的人一样,这些小鼠活到了成年,但运动功能障碍恶化,外周轴突缺失,重要的是,一种叫做巨噬细胞的免疫细胞浸润。
研究人员惊讶地发现,减少巨噬细胞的数量逆转了小鼠的轴突损失和疾病症状。该研究表明,SARM1不仅直接导致轴突损失,而且还在驱动神经炎症中发挥作用,而神经炎症只会加剧问题。研究结果还表明,一些神经退行性疾病可以用阻断巨噬细胞或其他炎症免疫细胞的免疫调节药物治疗。
在第二篇论文中,研究人员调查了SARM1在Charcot-Marie-Tooth病2a型中的可能作用。Charcot-Marie-Tooth病是一种常见的遗传性周围神经病变,也是一般研究轴突丢失的良好模型。这种疾病的患者会逐渐丧失运动和感觉轴突,并出现行走困难,肌肉无力以及手脚有刺痛或灼烧感。这种疾病是由线粒体中一种重要蛋白质的突变引起的,线粒体是细胞的能量工厂。这种突变发生在一种叫做mitofusin2的蛋白质中,它会损害线粒体的正常功能。许多研究都集中在异常的线粒体上,认为它们一定是这种疾病的根源。
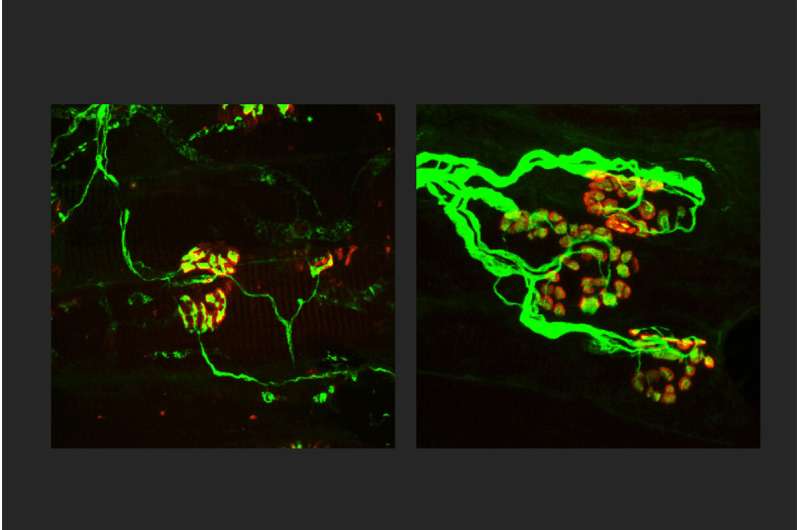
令人惊讶的是,研究人员发现,在患有2a型腓骨marie - tooth病的啮齿类动物模型中删除SARM1可以阻止动物表现出的大多数问题——独立于患病的线粒体。消除SARM1阻断或延缓轴突死亡、肌肉萎缩、线粒体异常和神经肌肉连接(神经元与肌肉的界面)问题。即使有突变的mitofusin2蛋白存在,删除SARM1也能保护线粒体免于进一步退化和功能障碍。
“当我们阻断SARM1时,我们不仅保护了轴突,我们还得到了更健康的线粒体,”DiAntonio说。“这完全是一个意外,但我们希望它能与许多以线粒体损伤为中心的神经退行性疾病有关,如帕金森症。疾病,因为很多神经退行性疾病有线粒体功能障碍的成分。”
进一步探索
Caitlin B. Dingwall等,巨噬细胞损耗阻断先天性sarm1依赖性神经病,临床调查杂志(2022)。DOI: 10.1172 / JCI159800