研究人员确定了研究治疗多发性硬化症进展的模型
加州大学洛杉矶分校研究人员的一项新研究发现了一种动物模型,可用于研究改善多发性硬化症患者残疾的治疗方法。
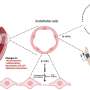
多发性硬化症(MS)是一种自身免疫和神经退行性疾病,患者的免疫系统攻击大脑和神经脊髓.针对免疫机制和减少多发性硬化症复发的治疗方法有很多,但没有一种是旨在保护大脑和脊髓细胞免受损伤的。现有的治疗方法在减缓残疾积累方面的效果有限,而且没有一种治疗方法能真正改善残疾。
确定…的动物模型疾病进展是找到更好治疗方法的关键一步,因为疾病发展的潜在机制可以被识别并阻断。
Rhonda Voskuhl博士是UCLA多发性硬化症项目的主任,Allan Mackenzie-Graham博士是神经学的副教授,他们发现了一种动物模型与进展性多发性硬化症有许多相似之处。
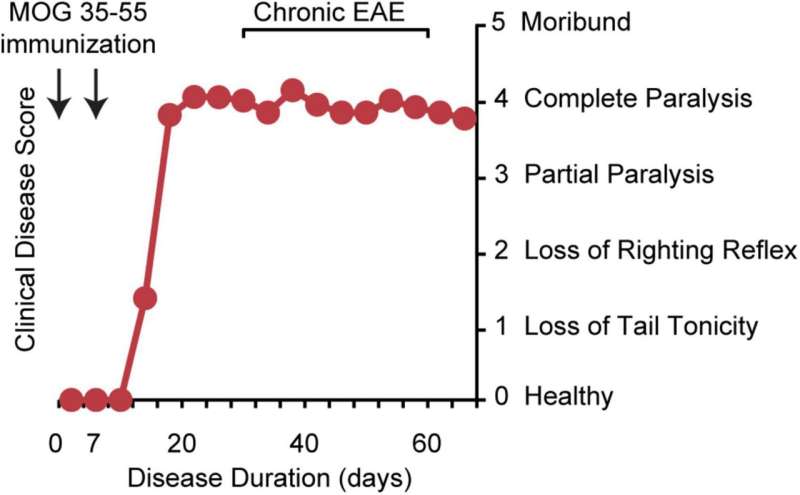
以前,急性和复发型实验性自身免疫性脑脊髓炎(EAE),一小鼠模型以血液和脊髓内炎症为特征,在目前多发性硬化症抗炎治疗的发展中发挥了核心作用。
在这里,Voskuhl和MacKenzie-Graham报告了慢性EAE的大脑MRI和神经病理学分析,揭示了许多与ms共享的神经退行性变特征大脑皮层小脑和视神经等。
在未来,这个模型可以被研究人员用来发现改善多发性硬化症的行走、认知、协调和视觉障碍的治疗靶点。
这项研究发表在分子神经科学前沿这是关于进行性多发性硬化症模型需求的系列文章的一部分。
进一步探索