阿尔茨海默症风险基因破坏了大脑“线路”的绝缘
众所周知,携带一个APOE4基因变体副本的人患阿尔茨海默氏症的风险会增加三倍,携带两个副本的人患阿尔茨海默氏症的风险会增加约十倍,但其根本原因以及如何帮助患者仍基本未知。11月16日,麻省理工学院的一个研究小组发表了一项研究自然提供了一些新的答案,作为更广泛的研究的一部分,这些研究已经证明了大脑中不同细胞类型的APOE4的后果。
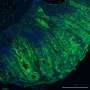
这项新研究结合了来自死后人类大脑的证据大脑细胞培养和阿尔茨海默氏症模型小鼠,以表明当人们有一个或两个APOE4副本,而不是更常见和风险中性的APOE3版本时,细胞少突胶质细胞对胆固醇的管理不善,无法将脂肪分子输送到长如藤蔓的轴突“线路”上,而神经元则通过轴突“线路”来连接大脑电路。这种被称为髓磷脂的脂肪绝缘体的缺乏可能是阿尔茨海默病的病理和症状的重要原因,因为没有适当的髓磷脂,神经元之间的通信就会退化。
由皮考尔教授、麻省理工学院皮考尔学习与记忆研究所和衰老大脑计划主任蔡黎慧(Li-Huei Tsai)领导的研究小组最近的研究发现,APOE4以独特的方式干扰脂肪分子或脂类,而脂类是由包括神经元、星形胶质细胞和小胶质细胞在内的关键脑细胞类型处理的。在这项新研究和之前的研究中,该团队已经确定了在实验室中出现的可以纠正这些不同问题的化合物,从而产生了潜在的基于药物的治疗策略。
这项新研究不仅通过发现APOE4如何破坏髓鞘形成,还通过使用单核RNA测序(snRNAseq)对主要脑细胞类型进行了首次系统分析,从而扩展了这项工作基因表达APOE4基因携带者和APOE3基因携带者的差异
麻省理工学院大脑与认知科学学院的蔡教授说:“这篇论文非常清楚地从死后人脑的snRNAseq基因型特异性中显示,APOE4对不同脑细胞类型的影响非常明显。”“我们看到脂质代谢的收敛被打乱,但当你真正深入研究不同类型的脑细胞中被打乱的脂质途径时,它们都是不同的。
“我觉得脂质失调可能是我们观察到的许多病理的基础生物学,”她说。
这篇论文的主要作者是Joel Blanchard,他是西奈山伊坎医学院的助理教授,在蔡的麻省理工学院实验室做博士后,Djuna Von Maydell和Leyla Akay是蔡实验室的研究生,Jose Davila Velderrain是Human Technopole的研究小组负责人,也是麻省理工学院计算机科学教授Manolis Kellis的实验室的前博士后。
有许多检查髓鞘形成的方法
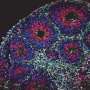
死后的人类大脑样本来自宗教秩序研究和匆忙记忆和衰老项目。该团队的snRNAseq结果,是冯·梅德尔制作的数据集免费提供该研究涵盖了来自32人前额皮质的11种不同类型的超过16万个单个细胞,其中12个含有两个APOE3副本,12个含有APOE3和APOE4各一个副本,8个含有两个APOE4副本。APOE3/3和APOE3/4样本根据阿尔茨海默病诊断、性别和年龄进行了平衡。所有APOE4/4携带者都患有阿尔茨海默症,8人中有5人是女性。
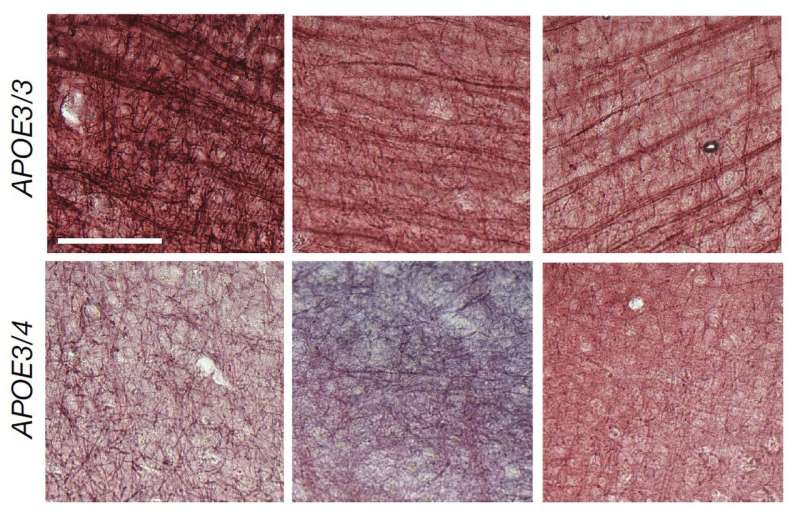
一些结果反映了已知的阿尔茨海默病的病理,但其他的模式是新的。其中一项研究表明,携带apoe4的少突胶质细胞表现出更高的胆固醇合成基因表达和胆固醇运输中断。人们的APOE4拷贝越多,影响就越大。这是一个非常有趣的结果之前的分析该研究发现,阿尔茨海默病与少突胶质细胞中髓鞘化基因表达减少有关。
通过使用各种技术直接观察组织,研究小组发现在APOE4大脑中,异常量的胆固醇在细胞体内积累,特别是在少突胶质细胞中,但在神经轴突周围相对缺乏。
为了了解原因,研究小组使用患者来源的诱导多能干细胞,创建了实验室细胞培养的少突胶质细胞,通过工程改造,使其仅因是否具有APOE4或APOE3而不同。APOE4细胞再次出现严重的脂质破坏。特别是,受影响的少突胶质细胞在体内囤积了额外的胆固醇,有迹象表明,额外的内部脂肪对内质网的细胞器造成了压力,内质网在胆固醇运输中起着重要作用,确实减少了向细胞膜运输的胆固醇。之后,当它们与神经元共培养时,APOE4少突胶质细胞不能像APO3细胞那样使神经元髓鞘化,无论神经元是否携带APOE4或APOE3。
研究小组还观察到,在死后的大脑中,APOE4携带者的髓鞘形成要少于APOE3携带者。例如,在APOE4大脑中,贯穿胼胝体(连接大脑半球的结构)的轴突周围的鞘明显更薄。在携带人类APOE4基因的小鼠和携带APOE3基因的小鼠中,情况也是如此。
有效的干预
急于找到一种潜在的干预手段,研究小组将注意力集中在影响胆固醇的药物上,包括抑制胆固醇合成的他汀类药物和帮助胆固醇运输的环糊精。他汀类药物没有帮助,但将环糊精应用于培养皿中培养的APOE4少突胶质细胞,减少了细胞内胆固醇的积累,并改善了与神经元共培养的髓鞘形成。此外,它对APOE4小鼠也有这些作用。
最后,研究小组用环糊精治疗了一些APOE4小鼠,而不治疗其他小鼠,并对它们进行了两种不同的记忆测试。经环糊精处理的小鼠在两项测试中的表现都明显更好,这表明髓鞘形成的改善与认知能力的改善之间存在关联。
Tsai说,一幅清晰的图景正在显现,通过细胞类型干预纠正特定的脂质失调可能有助于抵消APOE4对阿尔茨海默病的作用。
蔡说:“令人鼓舞的是,我们已经看到了一种挽救实验室和小鼠模型少突胶质细胞功能和髓鞘形成的方法。”“但除了少突胶质细胞,我们可能还需要找到临床有效的方法来照顾小胶质细胞、星形胶质细胞和血管系统,以真正对抗疾病。”
除了Tsai和Kellis两位主要作者外,该论文的其他作者还有Hansruedi Mathys、Shawn Davidson、Audrey EffenbergerChi0yu Chen、Kristan Maner-Smith、Ihab Jahhar、Eric Orlund、Michael Bula、Emre Agbas、Ayesha Ng。、蒋学乔、马丁·卡恩、克里斯蒂娜·布兰科-杜克、尼古拉斯·拉沃伊、刘力旺、里卡多·雷耶斯、林元塔、Tak Ko、Lea R'Bibo、威廉·雷尔文纽斯、大卫·班纳特和休·卡姆。