新发现的乳腺癌扩散分子显微镜
新技术可以跟踪的乳腺癌细胞负责疾病的传播,第一次突显出肿瘤细胞可能是一样重要的位置突变肿瘤的生长。
方法是由一个团队从威康桑格研究所EMBL的欧洲生物信息学研究所(EMBL-EBI),德国癌症研究中心(是,DKFZ),生命的科学实验室在瑞典,和合作者。它可以用来帮助癌症回答的一些大问题,比如为什么有些癌症细胞扩散,治疗抵抗是如何形成的,以及为什么一些治疗失败。
这项新的研究,发表在自然显示,现在可以如何映射肿瘤是如何发展,结合肿瘤细胞的遗传信息,周围的细胞类型,以及如何与环境互动。
在未来,这种方法可以用来看看治疗不仅影响癌症基因水平,而且任何对肿瘤与如何相互作用的影响免疫系统和它周围的环境。
乳腺癌是最常见的癌症之一,在英国,有55500名女性和370名男性被诊断出。
乳腺癌通常开始于细胞开始肆意地生长,通常由于突变细胞。加班肿瘤变成了的细胞,称为癌克隆,每个都有不同的基因突变。因为它们是基因不同,他们可以对治疗的反应不同。例如,一些癌症细胞可以治疗产生耐药性,或一些可能蔓延到全身。
所发生的突变会影响周围所发生的癌症,细胞包围着,和人的免疫系统。因此,能够研究环境,癌症细胞,出现突变,癌症细胞扩散至全身,给肿瘤演化的完整视图。
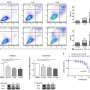
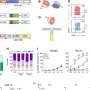
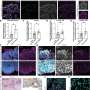
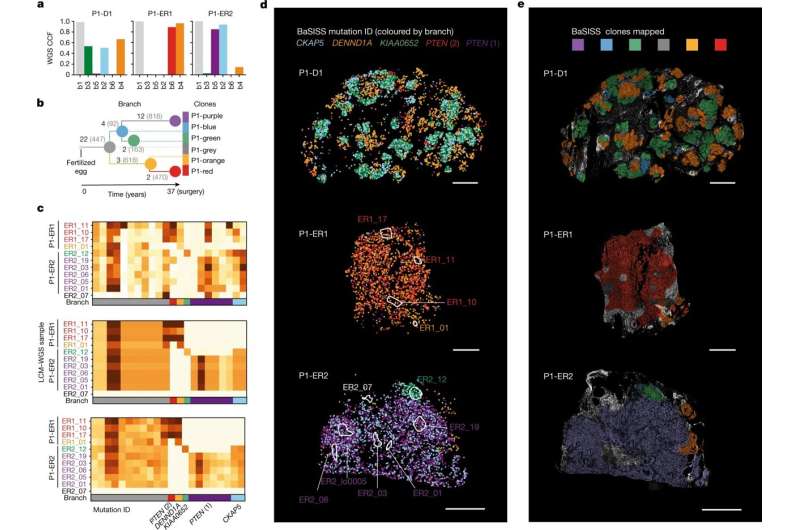
这种新技术,由基金会桑格研究所的研究人员,EMBL-EBI, DKFZ,生命的科学实验室,和合作者,使用成千上万的微小的荧光分子探针来研究细胞DNA和RNA并使用荧光显微镜扫描大块组织。癌症基因和身体映射出一个独特的克隆,基因表达程序变化和展示他们如何与环境互动。
Artem Lomakin,第一作者从EMBL的欧洲生物信息学研究所(EMBL-EBI)和德国癌症研究中心(是,DKFZ)说,“我们已经创建了一个系统,它结合了进化计算和实验技术,允许我们地图癌症血统在自然栖息地的人体组织。”
“虽然之前已经可以跟踪血统的癌症肿瘤细胞在实验设置中,这是第一次,多个血统追踪在人体组织中,完整的概述乳腺癌在体内发展。见解之前由我们的系统是不可能的,特别是在这种规模。”
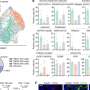
研究小组发现,在多个阶段的乳腺癌发展有特定的,和经常出人意料,模式的克隆生长和基因克隆不同取决于在乳房开始。
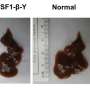
结果还表明,有时不仅仅是影响肿瘤生长的基因,而且肿瘤的位置。在这种情况下,基因可以作为一个工具来找到更多关于发生了什么情况导致癌细胞克隆传播到全身。
垫尼尔森教授,文章的第二作者从斯德哥尔摩大学生命科学实验室,说:“癌症是由基因突变引起的细胞,本研究是第一次我们可以使用DNA基础特定的探测目标的这些突变在一组癌细胞克隆。”
“这种创新技术允许我们准确地重建这些克隆的蔓延。一个重要的我们的研究暗示,它可能不是单独的基因改变的原因,癌细胞生存和传播;也可能是他们在哪里。这增加了额外的一层复杂性以及新的潜在目标疾病的方法。这也可能解释为什么一些治疗方法只在一些人工作,即使他们有类似的突变,随着肿瘤在乳房的不同区域。”
在将来,它有可能发展疗法可以预防或减轻癌症生长和扩散的能力,通过影响肿瘤周围的环境。除此之外,研究人员可以使用新开发的工具来测试新的治疗方法如何影响癌症和与免疫系统的相互作用,给出一个完整的治疗工作和任何可能的副作用。
莫里茨Gerstung教授,文章的第二作者德国癌症研究中心(是,DKFZ)说:“测序癌症肿瘤可以给我们一个很好的了解肿瘤的遗传多样性。但激动人心的关于这个技术是第一次,我们可以看到环境如何塑造癌症进化。”
“我们能够看到哪些癌症克隆进展变得更积极,不,这将使我们能够更好的了解什么是关键步骤肿瘤的生长,以及我们如何减轻或预防疾病。”
露西耶茨博士从威康基金会桑格研究所的文章的第二作者,说:“我们的研究提供了一个工具,可以追溯到乳腺癌细胞继续导致肿瘤在身体的其他部位,并能帮助回答癌症的一些重大问题,如为什么一些癌症细胞传播和一些不喜欢。”
“完全理解,因此治疗乳腺癌,我们需要能够看到整个癌症在体内如何相互作用,与周围的细胞,并与免疫系统。这项新技术结合多种技术和专业知识,结合不同的方法给一个完整的视图的癌症以前没有可能。”
更多信息:露西耶茨,空间基因组地图的结构、性质和演化的癌症克隆,自然(2022)。DOI: 10.1038 / s41586 - 022 - 05425 - 2