新的数据表明,COVID疫苗设计思路具有更好的变异弹性

最新研究结果表明,疫苗诱导的针对SARS-CoV-2的中和抗体主要针对病毒进入机制的两个主要区域之一。
研究结果还指出了同一域的关键作用斯派克在引起广泛的抗体反应对许多变种,以及相关的病毒。
这两项发现为临床开发抗变疫苗和sarbec病毒疫苗提供了策略,作为未来大流行准备工作的一部分。
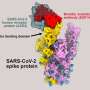
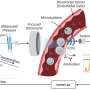
刺突蛋白赋予病毒冠状外观,为病毒进入宿主细胞提供了途径。刺突蛋白的一个亚基与上的受体结合宿主细胞并能识别何时发生了正确的着陆。
该钉还采用了加载弹簧的配置。当它迫使病毒与宿主细胞融合时,它的形状会发生变化,从而引发感染。
抗体试图通过结合到病毒刺突蛋白上的位点来抵御SARS-CoV-2对细胞的入侵。目前可接种的疫苗范围很广免疫系统美国自己对COVID-19的反应,可能会引发这种情况抗体.
由西雅图华盛顿大学生物化学副教授、霍华德休斯医学研究所研究员David Veesler领导的国际研究小组决定使用冷冻电子显微镜和其他方法观察刺突蛋白定向抗体反应的特异性。他们想评估抗体结合位点在对抗SARS-COV-2变体的中和活性方面的相对贡献。
通过这项研究和相关工作,他们想了解不同的刺突蛋白构象对血浆抗体中和活性的影响。这些信息可能有助于发现调节抗SARS-CoV-2抗体的大小和广度的方法。
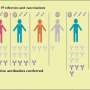
研究人员研究了没有接触过COVID-19,但接受了世界上使用最广泛的7种疫苗之一的初级系列剂量的个人的血浆样本。此外,他们还检查了有感染史和疫苗接种史的受试者的样本。他们还研究了2021年1月疫苗接种项目开始前感染COVID-19的人的恢复期血浆。
他们的研究结果发表在科学免疫学11月10日。这篇论文题为《SARS-CoV-2刺突构象决定由广泛的人类疫苗引起的血浆中和活性》。这篇论文的主要作者是维斯勒实验室的约翰·e·鲍恩。

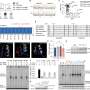
科学家们观察到,参与者血浆的体外病毒抑制活性与抗刺突蛋白预融合形式的抗体应答量之间存在很强的相关性。对所有评估的疫苗和以前感染引起的抗体都是如此。
研究人员写道:“我们观察到抗体中和活性和S1结合抗体反应之间存在类似的正相关,这表明S1靶向抗体在SARS-CoV-2中和中发挥了关键作用。”S1是参与宿主细胞受体接合的刺突蛋白单位,这是病毒攻击细胞的第一部分。
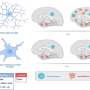
研究人员还发现,中和抗体血浆样本也对应于特异性靶向S1刺突蛋白单元上两个结构域的抗体的存在。早期的研究表明,这两个被命名为NTD和RBD的区域是在感染期间或接种疫苗后中和抗体反应的主要目标。
这些NTD和rbd导向的宿主抗体也可能部分解释了进化选择压力病毒的那些部分科学家们认为,这种选择压力可能导致变异体的突变迅速积累,以试图战胜这种免疫策略。
研究人员还发现,与瞄准NTD位点的抗体相比,针对许多SARS-CoV-2变体的抗RBD位点抗体的交叉中和抗体反应的广度更大。
研究人员指出:“多种广泛中和的sarbecavirus抗体可以识别不同的RBD抗原位点。”sarbecvirus是包括大流行冠状病毒在内的一大类病毒。
另一方面,靶向S2亚基,这是参与膜融合的突起的一部分,对疫苗诱导的中和活性没有太大贡献。这种抗体数量少,效力弱。
研究人员总结说,这一发现表明,开发基于rbd的针对SARS-CoV-2和更大组相关sarbeco病毒的疫苗作为未来大流行准备工作的一部分可能有用。