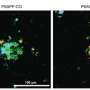
阿兹海默氏症试验药物的第二例死亡引起了人们的关注
目前已有两人死于脑出血,这可能与一种实验性阿尔茨海默病药物有关,这让人们对这种药物的安全性产生了怀疑。
最近,一名患有早期阿尔茨海默氏症的65岁妇女死于大量脑出血,一些研究人员将其与一种抗体药物lecanemab联系起来淀粉样β蛋白根据11月27日发表在科学内幕.
报道指出,这名女子中风,并出现了一种脑肿胀和脑出血,这是此前出现这种抗体的情况。
芝加哥西北大学医学中心的急诊室医生用一种普通但强力的破凝剂——组织纤溶酶原激活剂(tPA)来治疗这名妇女。她的大脑外层立刻大量出血。
她的丈夫说:“当他们把它注入她体内时,她的身体就像着火了一样。科学内幕.“她在尖叫,大概有八个人才把她按住。太可怕了。”
病例报告称,这名女子几天后去世。
在此之前,一名80岁的男性患者也死亡,他当时正在参加lecanemab的3期临床试验。他的死亡可能与实验药物与一种叫做阿哌沙班(Eliquis)的血液稀释剂相互作用有关。
西北大学的神经病理学家鲁道夫·卡斯特拉尼(Rudolph Castellani)对这名女子进行了尸检,他断定她已经死亡淀粉样蛋白沉积环绕着她大脑的许多血管。
Castellani说,这名女子每两周注射一次lecanemab,这似乎使她的血管发炎并削弱。当这些血管暴露在破凝剂下时,就会破裂,即使在传统的中风病例中也会发生这种情况。
卡斯特拉尼说:“这是一记连击。科学内幕。“毫无疑问,这是一种由治疗引起的疾病和死亡。如果这个病人没有服用lecanemab,她今天可能还活着。”
如果获得批准,lecanemab将成为第二种治疗阿尔茨海默症患者的抗淀粉样蛋白药物。
第一种是Aduhelm (aducanumab),它不顾评论家和研究人员对药物有效性的质疑,获得了美国食品和药物管理局(fda)的批准。
日本卫井公司(Eisai Co.)定于本周提供lecanemab三期试验的首份详细报告,该试验包括了约1,800名有早期阿尔茨海默氏症症状的患者。
卫材与瑞典公司BioArctic共同开发了lecanemab,并与美国生物科技公司Biogen共同赞助了临床试验。
一个新闻发布会上该公司9月份发布的一份报告称,服用lecanemab的人淀粉样蛋白减少了27%认知能力下降比18个月期间服用安慰剂的人要多。
卫材公司拒绝就该女子的案件置评,科学内幕说。
该公司在一份报告中说:“所有现有的安全信息表明,lecanemab疗法与整体或任何特定原因的死亡风险增加无关。声明.
在18个月的试验中,该妇女可能服用了lecanemab或安慰剂,但她在死亡前一个月肯定服用了这种药物。她选择接受它作为临床试验开放标签扩展的一部分。
这名女性和男性都患有广泛性脑淀粉样血管病(CAA),这种情况下,淀粉样沉积逐渐取代了血管壁的平滑肌。
专家向科学内幕在这类患者中,剥离淀粉样蛋白——就像像lecanemab这样的药物所要做的那样——可以削弱血管如果暴露在血液稀释剂或凝块阻断剂中,他们就容易出血。
报告指出,近一半的阿尔茨海默病患者患有CAA,许多人还患有心脏疾病,通常用血液稀释剂治疗。
西奈山有更多脑淀粉样血管病.
版权所有©2022每日健康.版权所有。