细胞外黏度与癌症扩散有关

新的研究结果表明,包围细胞的细胞外液的黏度(或流动阻力)越高,癌细胞就越容易从原发肿瘤转移到身体的其他部位。
我们破译了其中的奥秘细胞该研究的首席研究员、生物医学工程和肿瘤学William H. Schwarz教授、约翰霍普金斯大学Kimmel癌症中心侵袭和转移项目成员、化学和生物分子工程威廉H.施瓦茨教授说。
“我们还表明,当预先暴露在升高的液体粘度中时,细胞有能力形成记忆。我们相信,这些发现将迫使癌症机械生物学以外的其他领域的研究人员考虑流体粘度作为调节的关键物理线索细胞反应."
这些发现揭示了一种促进癌细胞扩散的新机制,发表在11月2日的自然并为正在进行的研究提供一个框架,这些研究可能最终导致识别出抗击癌症转移的潜在新靶点。
Konstantopoulos实验室最近的毕业生、该研究的第一作者Kaustav Bera博士解释说,尽管近半个世纪以来,人体体液的粘度被认为与许多疾病相关,但迄今为止,关于癌细胞扩散的研究主要是使用类似于水的低粘度液体进行的。“我们的预期是,由于在更粘稠的流体中阻力更大,癌症细胞不会有效地转移或转移,但我们证明事实恰恰相反。”她说。
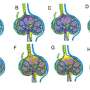
研究人员揭示了细胞如何感知和响应高粘度的物理线索,以及控制细胞形状和细胞内组织并参与细胞运动的细胞骨架如何与离子通道和离子转运体(引导带电分子穿过细胞膜的蛋白质)合作,以调节高粘度下的高效迁移。
细胞外黏度随着正常细胞和癌细胞分泌的大蛋白的降解以及淋巴管的引流受阻而上升原发肿瘤增长。研究人员发现,更高的阻力环境驱动更密集的肌动蛋白网络的形成,促进离子转运体的局部富集,离子转运体与水通道合作,促进水的吸收,促进细胞膨胀,增加膜张力。
在细胞的前缘,膜张力的增加激活了信号通路其中包括一个被称为TRPV4的离子通道,可以感知物理信号。液体粘度指示细胞打开TRPV4通道,促进钙的摄入,从而增强细胞的发力能力,最终推动细胞更快运动。
西班牙巴塞罗那Pompeu Fabra大学的研究合著者Selma Serra博士说:“这就像细胞在高粘度的情况下去健身房进行高强度训练和发展肌肉(肌动蛋白和肌球蛋白),这提高了它们的性能,从而更快地到达最终目的地。”
以前人们认为机械感应级联始于离子通道比如TRPV4,博士后研究员、该研究的第二作者亚历克斯·基帕斯博士说。他说:“我们发现黏度感知始于更密集和高度分支的肌动蛋白的形成,TRPV4的激活实际上是在肌动蛋白的下游。”
当研究人员敲除TPRV4时,它们阻断了细胞的快速运动,以及细胞在预暴露于高粘度环境时形成记忆的能力。研究人员使用3天大的斑马鱼胚胎模型来证明,提高黏度的记忆可以使细胞在活体血管中更快地移动。
他们还用鸡胚胎和小鼠模型证明,记忆可以通过一个被称为外渗的过程,增强癌细胞向血管外扩散,并导致更多的远处转移菌落。
Konstantopoulos说,在实验室动物模型中,研究原发肿瘤和从原发肿瘤扩散的癌细胞如何在疾病进展和侵入组织微环境过程中对细胞外液粘度的局部变化作出反应,这将是有意义的。
开发和优化生物传感器,使实时测量细胞外液粘度和成像活动物的癌细胞将是解决这一问题的关键。他们还计划调查是否细胞外粘度影响其他生理相关的细胞过程。