研究人员开发了一种新的砍刀技术来切割癌症基因组并研究拷贝数的变化
人们已经把它叫做砍刀纸了。
尽管如此,斯隆凯特林研究所的主要作者弗朗西斯科·“潘乔”·巴里加和卡洛扬·查诺夫不希望他们的新研究技术的名字掩盖了他们的发现,这些发现揭示了一种新的疾病基因变化这约占所有癌症的15%,这可能有助于识别可能对免疫疗法有反应的患者。
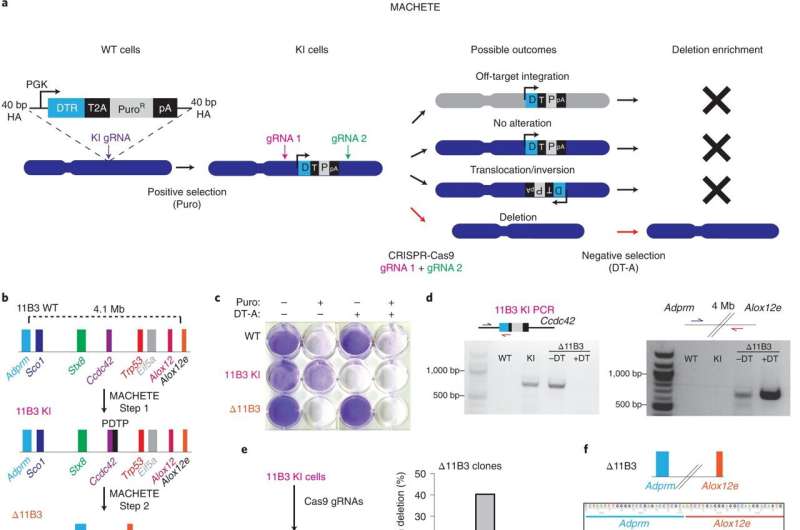
MACHETE是他们开发的一种基于crispr的方法,用于研究拷贝数改变(cna),这是癌症中经常发生的大规模基因变化。
MACHETE的首字母缩写是染色体的分子改变与工程串联元素。这是一种新的方法,可以切割出遗传密码的重要目标部分,以反映癌症和其他人类疾病中出现的变化。
这意味着第一次有了一种直接而有效的方法来研究实验室模型中的CNA缺失——比如他们在《柳叶刀》杂志上发表的研究中使用的胰腺癌和黑色素瘤小鼠模型自然癌症2022年11月7日。
“一开始,我们甚至不想把MACHETE放在我们的论文标题中,以更好地突出我们发现的迷人生物学,”该研究所的博士后巴里加博士说,该研究所是纪念斯隆·凯特琳癌症中心(MSK)的实验研究部门。
尽管如此,这并没有阻止一位实验室伙伴在他第一次展示作品后,在他的桌子上贴了一张著名的丹尼·特雷霍(Danny Trejo)角色砍刀(Machete)的照片。也不会有其他科学家通过这位演员的推特账号发布论文预印本的副本。(唉,这个手势没有得到回应。)
不仅仅是单基因癌症突变
为了理解这项研究在人类癌症中最常见的拷贝数改变之一方面取得了新的突破,以及它对未来患者可能意味着什么,人们需要欣赏潜在的生物学。
许多人认为癌症的突变是基因密码中的小“错别字”,它会影响单个基因的活动——要么激活它,要么关闭它。几十年来,研究人员也主要关注这些导致多种癌症的微小错误。
然而,拷贝数的改变可以同时影响几十个基因,复制或删除单个染色体的大部分。
研究人员指出,一个典型的肿瘤平均携带24个不同的cna,影响其基因组的30%。
Tsanov博士说:“点突变相对来说比cna更容易研究。”Tsanov博士和Barriga博士一样,是研究员Scott Lowe实验室的博士后,Scott Lowe是该研究的资深作者和研究所癌症生物学与遗传学项目的主席。“但cna同样重要——只是要复杂得多。”
MSK先前的研究发现,具有较高水平的CNA的肿瘤(也称为CNA负担)与乳腺癌、前列腺癌、子宫内膜癌、肾透明细胞癌、甲状腺癌和结直肠癌的复发和更坏的结果有关。
但是,同样,这些变化的大小和种类——影响数千甚至数百万个DNA碱基对,而不仅仅是DNA序列中一个字母的改变——使得它们很难在实验室模型中重新产生以进行仔细研究。
巴里加博士在从实验室乘罗斯福岛电车回家的路上,想到了一种研究大规模基因缺失的潜在新方法。
“我想知道:‘我们如何选择具有预期缺失的细胞,即使它们非常罕见?’”他说。“那天晚上,我有了一个想法,并草拟了总体战略的初步概念。当我们尝试的时候,它成功了。在我接下来的职业生涯中,我可能再也不会有这么顺利的事情发生了。”
他开玩笑说,想出正确的单词组合让MACHETE这个缩写词起作用花了更长的时间。不过,当用MACHETE在一只患有胰腺导管腺癌的小鼠模型上进行基因改变,其结果与沙诺夫博士在另一个项目中研究的另一只小鼠模型上自然发生的类似突变相同时,两人知道自己有所发现。
“从那以后,我们真的是密切合作,”查诺夫博士说。该研究团队还包括来自MSK、安大略省癌症研究所、纽约大学格罗斯曼医学院和多伦多玛格丽特公主癌症中心的十多名其他科学家。
研究可能有助于确定哪些患者将受益于免疫疗法
经过基因“切割”的细胞被插入实验室小鼠的胰腺后,小鼠患上了癌症。基因改变删除了9号染色体的一个片段,以及一个被称为cdkn2a的基因——一个公认的肿瘤抑制基因。正如预期的那样,这关闭了细胞防止肿瘤细胞出现的先天能力。
这一广泛切片也去除了一组干扰素的遗传密码,干扰素是一种触发免疫细胞抗击癌细胞等入侵者的蛋白质,科学家们想要测试干扰素的重要性。
人类中最常见的一种cna影响这一染色体区域- 9p21.3,大约一半患有这种疾病的患者在肿瘤中也缺少这些干扰素。
“我们已经知道CDKN2A突变很长时间了,它们的工作方式已经很引人注目了,”霍华德·休斯医学研究所研究员洛博士说。“这项研究表明,它还有更多的意义,具有重要的治疗意义。”
干扰素的额外损失形成了一种组合拳,使肿瘤对防御者不可见免疫系统研究人员发现,这有助于癌症扩散。
“很难研究这些干扰素,因为它们是由16个基因组成的集群编码的,”洛博士补充道。“使用MACHETE揭示了发展中的癌细胞避免被免疫系统识别的主要方式,这也可能导致对旨在重新激活免疫系统以攻击癌症的免疫疗法产生耐药性。”
共同作者Dana Pe'er是斯隆凯特林研究所的计算生物学家,她在帮助团队了解干扰素基因的破坏是如何影响的方面发挥了重要作用免疫细胞帮助癌症逃避免疫系统,洛博士说。
除了胰腺癌,这一发现也适用于黑色素瘤的小鼠模型。
因此,这项研究表明,干扰素区域仍然完整的患者可能比那些失去干扰素区域的患者更适合进行免疫治疗。免疫疗法可以创造奇迹,但最大的挑战之一是确定哪些患者的癌症会对免疫疗法产生反应,哪些不会。
然而,即使是尖端的基因组测试,如MSK-IMPACT,通常也不会收集有关这组干扰素基因的信息。进一步的研究可能会显示,将其添加到测序测试中是否有助于识别更有可能从中受益的患者免疫疗法洛维博士指出。
同时,CNA缺失与多种称为染色体缺失综合征的人类遗传疾病有关。“因此,MACHETE为研究大型删除事件提供了一个新的框架癌症巴里加博士说,并指出其他六个研究小组已经在使用斯隆凯特林研究所开发的技术。