机器学习可以帮助预测病人对癌症免疫疗法
预测哪些病人会对治疗反应良好是进退两难的境地,癌症免疫治疗领域超过四十年。现在,约翰霍普金斯Kimmel癌症中心研究人员及其彭博~ Kimmel癌症免疫疗法更近一步解决这个问题。在一项小型研究,他们成功地训练机器学习算法来预测,事后看来,黑素瘤患者应对治疗和没有回应。
DeepTCR开源程序,作为预测临床证明是有价值的工具,但它也充当一个强大的教师,教学研究人员对病人的生理机制对免疫治疗的反应。
说:“DeepTCR的预测能力是令人兴奋的,约翰·威廉·Sidhom,医学博士博士,这项研究的第一作者,“但是我发现更有趣的是,我们能够视图的模型了解免疫系统对免疫治疗的反应。我们现在可以利用这些信息来开发更健壮的模型,可能还有更好的治疗方法,对许多疾病,即使是那些以外的肿瘤。”
总结的研究发表在《华尔街日报》科学的进步。
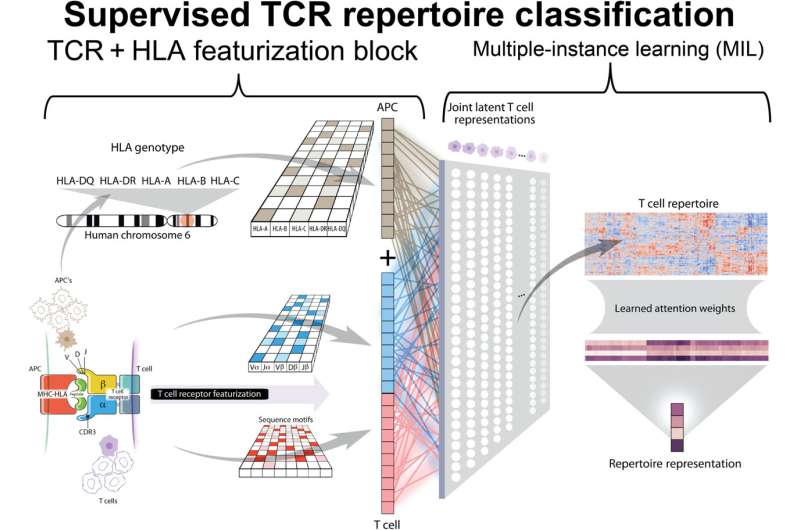
DeepTCR开发在约翰霍普金斯大学医学院的Sidhom当他是一个医学博士/博士学位。学生。它使用深度学习,人工智能的一种形式,在大量数据的识别模式。在这种情况下,数据是蛋白质的氨基酸序列称为T细胞受体(tcr)。
tcr坐在外免疫系统的T细胞,等待了敌人的一种蛋白质:癌症、细菌或病毒。细胞就像锁,只能通过一个键打开。T细胞的表面镶嵌着许多细胞,但是他们都是相同的,都是打开同样的敌人的关键。不知道敌人存在,许多不同的T细胞在体内。当细胞被激活,其T细胞释放分子杀死敌人,和它克隆自己来增强响应。
不幸的是,一些肿瘤细胞开发的方式阻止T细胞的反应,即使细胞被激活。目前免疫治疗药物,被称为检查点抑制剂,包括蛋白质阻碍这种能力在肿瘤,导致T细胞对癌症。然而,这些药物帮助只有少数的病人。
在当前的研究中,Sidhom,现在居民,将军038年临床试验期间收集的材料使用,测试一种免疫治疗药物的疗效(nivolumab)相比,结合两个(nivolumab和ipilimumab) 43不实用的黑色素瘤患者。肿瘤活检,包含一个数组的浸润T细胞,治疗之前和期间。
在将军的研究中,患者未见显著差异单药和联合用药。有些病人在两组和其他人没有回应。
使用的协议,Sidhom使用高科技基因测序发现周围每个肿瘤细胞剧目通过确定每个切片细胞的类型和数量。然后美联储数据DeepTCR计划,告诉它数据集属于急救员和nonresponders。然后该算法寻找模式。
研究者们首先问过如果有不同的免疫疗法治疗TCR体验反应者和nonresponders。算法识别的差异是预测患者的反应称为biomarkers-molecular用于指导治疗肿瘤的特征。然而,在该算法可以用于指导临床治疗,研究人员需要确认这些发现在一个更大的患者人群。
“精确基于免疫微环境在肿瘤免疫治疗指导治疗方案的最佳选择是至关重要的对于每一个病人,”德鲁Pardoll说,医学博士博士,教授,主任肿瘤学和彭博社~ Kimmel癌症免疫疗法。
“这些DeepTCR发现定义一个新的维度预测肿瘤的免疫反应检查点封锁deconvolute通过应用一种新的人工智能策略的大量受体表达的肿瘤浸润T细胞免疫的关键组件负责直接杀死肿瘤细胞。”
接下来,Sidhom想知道急救员和nonresponders之间的差异。他用另一项研究的数据与特定细胞(被他们的氨基酸序列)敌人蛋白质激活它们。数据集内的成千上万的细胞,每个回应不同的蛋白质从各种各样的入侵者:流感病毒,巴尔病毒,黄热病病毒和肿瘤。
发现是违反直觉的:患者对免疫疗法是那些有较高的特异性T细胞的肿瘤。Nonresponders有更多的肿瘤特异性T细胞。
观察细胞的变化能每个病人治疗后开始,Sidhom得知nonresponders周转率较高T细胞。“急救员和nonresponders有相同数量的肿瘤特异性T细胞疗法之前和期间,”他说。
”的身份T细胞反应者保持不变,但在nonresponders,有不同种类的T细胞疗法之前和期间。我们的假设是,nonresponders大量无效的肿瘤特异性T细胞从一开始。免疫治疗开始的时候,他们的免疫系统中发送一批新的T细胞,试图找到一个有效的,但是功能障碍依然存在。另一方面,救援人员已从发病有效的T细胞,但其抗肿瘤活性被肿瘤。免疫治疗开始时,它释放封锁,允许他们做他们的工作。”
”的应用深度学习框架在DeepTCR描述细胞的T细胞可以改善病人预后以及模型的分层explainability识别预测功能,”医学博士说,亚历山大•巴拉博士,病理学副教授约翰霍普金斯大学医学院的主任和精密医学信息学约翰霍普金斯Kimmel癌症中心。
Sidhom说DeepTCR算法的核心是一个“神经网络”,这是一个最简单的人工智能models-meaning很难了解学习模型。本文展示了如何使用甚至一个神经网络提取对其预测背后的生物学解释,”他说。“能力提供可辩解的AI将被证明是无价的癌症生物学和许多其他领域。”