抗体治疗如何影响COVID mRNA疫苗的广度

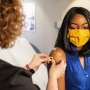
大流行已近三年,由于一两次感染、几剂mRNA疫苗或一轮单克隆抗体治疗,我们中的许多人现在都携带了抗病毒抗体。但并非所有的免疫反应都是平等的,我们最初产生抗体的方式可能会影响我们身体对SARS-CoV-2的反应特征。
现在,一项新的研究描述了在注射两剂mRNA疫苗之前接受单克隆抗体的个体所引起的独特免疫反应。这项研究发表在自然,探索了一种被称为抗体反馈抑制的现象,已知这种现象可以改变对某些病原体的免疫反应,同时有益地多样化人体对其他几种病原体的抗体库。研究结果表明,反馈抑制增加了COVID疫苗在先前接受单克隆抗体的人群中的覆盖率。
米歇尔·c·努森茨威格说:“反馈抑制可以增强免疫力,也可以抑制免疫力,这取决于病毒。”他与同事西奥多拉·哈齐扬努、保罗·比恩尼亚斯和玛丽娜·卡斯基共同领导了这项研究。“我们的研究结果表明,现有的SARS-CoV-2抗体可以使抗体反应多样化,这可能会增加mRNA疫苗的广度。”
豚鼠和抗体
抗体反馈抑制最早是由流行病学家Theobald Smith在世纪之交发现的,他证明了过量的抗体可以抑制豚鼠对白喉的免疫反应。这似乎是一个奇怪的转折——为什么被认为可以保护动物免受疾病侵袭的分子偶尔会关闭免疫系统下来吗?
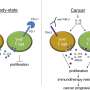
我们现在知道病毒有多个抗原表位——抗体用来识别病毒并锁定它的突出抗原片段。一旦人体对一种表位产生了强烈的抗体,免疫系统就会继续发展并多样化,而是产生附着在病毒其他部分的抗体。理想情况下,这增加了免疫反应的广度——例如,如果病毒发生突变,一个表位不再被识别,它可能仍然容易受到针对其他表位的抗体的攻击。
“抗体反馈可能是一件非常好的事情,”努森茨威格说。“你最终会收集到针对病毒许多不同部分的中和抗体,所有这些都是有帮助的。”
但在其他情况下,抗体反馈可能弊大于利。艾滋病病毒和流感病毒的表位数量都很有限,如果一个表位不能产生非常有效的抗体,那么一场完美风暴就会随之而来。一旦检测到剩余的最低有效抗体,身体就会停止这条线的生产,无意中阻碍了可能更好工作的类似抗体的生产。
Nussenzweig说:“HIV病毒上只有几个地方值得靶向,如果最初的反应阻断了这些表位,我们就不会得到广泛的中和反应。”
COVID中的抗体反馈
为了更好地了解抗体反馈如何影响COVID免疫,Nussenzweig和同事跟踪了接受单剂量单克隆抗体治疗的志愿者,后来又接受了两剂量mRNA疫苗。他们发现,这些志愿者与单独接种mRNA疫苗的人有明显不同的免疫反应。
两剂量的mRNA COVID疫苗通常会产生记忆B细胞的优势,它们表达针对刺突蛋白受体结合域的三个关键部分之一的抗体,如果没有这些部分,冠状病毒就无法感染细胞。正如预期的那样,Nussenzweig和同事们发现,从只接种疫苗的人身上获得的抗体中,约有一半针对所谓的第1、2或3类表位。
但在接种疫苗前接受单克隆抗体的志愿者体内,只有20%的抗体靶向这三种表位中的一种。相反,他们近80%的抗体针对受体结合域的第四部分,或其他表位。作者得出结论,反馈抑制在起作用——在单克隆抗体治疗导致产生针对第1、2或3类表位的抗体后,身体停止产生这些抗体,在接种疫苗后,转移到针对其他表位抗原表位.在这种情况下,影响是有益的。
“它们的免疫反应不同,但肯定不会更糟,”努森茨威格说。“事实上,接受单克隆抗体的个体受到了非常好的保护。”
研究结果表明单克隆抗体接种疫苗前接种疫苗可帮助多样化疫苗接种免疫反应通过增加mRNA疫苗的宽度来对抗COVID。也可能有重要的经验教训。“因为在受体结合域上有许多目标可以中和病毒在美国,抗体反馈非常有用,”Nussenzweig说。
以及驱动反馈的抗体盈余是否来自单克隆抗体或额外的疫苗他说,“抗体反馈对COVID非常好。”