三种以减缓衰老过程而闻名的方法被证明基本上无效
三种以减缓衰老过程而闻名的方法已被证明基本上无效。在他们的研究中,研究人员开发了一种新的方法来测量衰老,这解释了生物衰老的复杂性。
在这项新研究中,研究人员仔细研究了三种治疗人们普遍认为这些方法可以减缓衰老过程。然而,当测试时老鼠在美国,这些疗法在很大程度上被证明对延缓衰老无效。
这项研究的发起者、DZNE的丹·埃宁格博士总结道:“人体内部没有衰老时钟可以通过简单的开关来调节,至少在这里研究的治疗方式中是这样。”该团队开发了一种新的分析方法,可以测量对老化过程的影响。
这项研究的结果现在已经发表在该杂志上自然通讯,来自DZNE、Helmholtz Munich和德国糖尿病中心(DZD)的研究人员参与了这项研究。“我们为我们的干预选择了三个监管机构,许多专家认为这三个监管机构可以减缓衰老,”Martin hrabde Angelis教授解释说,他是实验遗传学研究所所长,也是慕尼黑Helmholtz德国小鼠诊所的主任,他也和他的团队一起推动了这个项目。
其中之一是间歇性禁食,在这种情况下消耗的卡路里会减少。第二个目标是细胞代谢的中心节点(mTOR),这也是所谓的“抗衰老药物”雷帕霉素的目标。第三个,反过来会干扰生长激素的释放。类似的治疗方法也被人类使用,尽管它们在衰老方面的功效尚未得到充分证明。
对于在小鼠身上进行的评估,科学家们对如何测量衰老这一问题提出了新的答案。DZNE的高级科学家丹·埃宁格(Dan Ehninger)解释说:“近几十年来,许多研究人员都将寿命作为衰老的间接衡量标准。”例如,老鼠能活到几岁?怎样才能延长寿命?
“人们通常认为,如果他们活得更久,他们的衰老速度也会更慢。但问题是,像许多其他生物一样,老鼠不会死于一般的衰老,而是死于非常特定的疾病,”Ehninger说。例如,高达90%的老鼠在年老时死于体内形成的肿瘤。“所以,如果你要观察整个基因组,寻找使老鼠长寿的因素,你会发现许多抑制肿瘤发展的基因,而不一定是在衰老过程中发挥一般作用的基因。”
因此,在他们的研究中,科学家们选择了一种不强调寿命的方法,而是专注于全面调查与年龄相关的各种身体功能的变化。“你可以把它看作是一项完整的健康状况调查,”马丁·赫拉普德·安吉利斯(Martin hrabde Angelis)说。
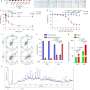
“健康检查的结果是一个涵盖生理学许多领域的数百个因素的纲要”——在检查时对动物状态的准确描述。
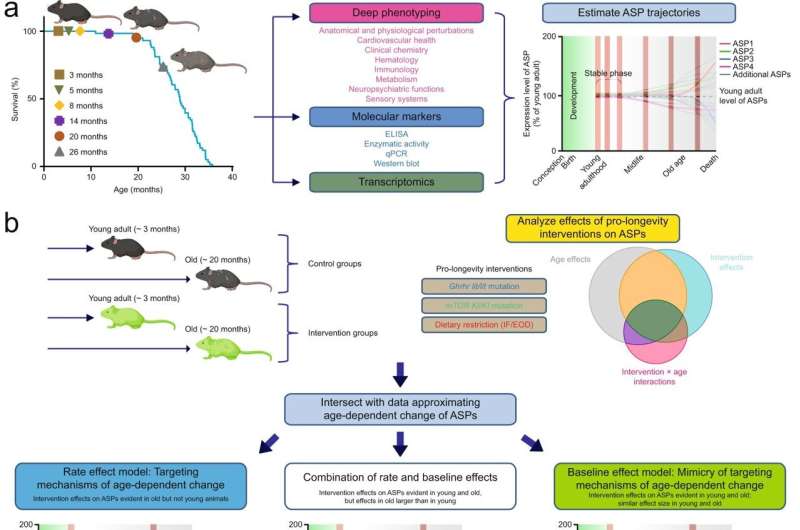
这正是研究人员对接受三种治疗方法之一的动物所采用的方法,这种治疗方法据称可以减缓衰老。在不同的生命阶段,他们进行了分析和比较:在生命的特定阶段,每个参数通常会发生多大的变化?当小鼠接受三种治疗中的一种时,参数的变化是否更慢?这研究设计这就有可能精确地确定是否天然衰老的过程可以减缓,重要生理功能也会随之恶化。
结果是明确的。尽管研究人员能够识别出年老老鼠看上去比实际年龄年轻的个别案例,但很明显,“这种影响不是由于减缓衰老,而是由于与年龄无关的因素,”丹·埃宁格(Dan Ehninger)说。“事实上,在健康指标出现年龄依赖性变化之前,一种治疗方法已经在年轻小鼠身上产生了效果,这证明了这些是补偿性的、一般的促进健康的作用,而不是针对衰老机制的。”
DZNE和Helmholtz糖尿病中心的团队现在已经把目光投向了下一个目标。他们希望研究专家认为可以延缓衰老的其他治疗方法。研究人员希望:新的研究方法将为可能的治疗方法及其有效性提供更全面的图景。