人工DNA杀死癌症:发夹状DNA与癌细胞中的microRNA结合,引发免疫反应
东京大学的研究人员使用人工DNA以一种全新的方式瞄准并杀死癌细胞。该方法在实验室测试中对人类宫颈癌和乳腺癌细胞以及小鼠恶性黑色素瘤细胞有效。
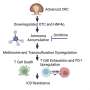
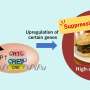
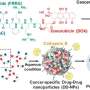
该团队制造了一对化学合成的发夹状,癌症造成DNA。当DNA对被注射到癌细胞中时,它们与某些癌症中过量产生的microRNA (miRNA)分子相连。一旦连接到miRNA,它们就会散开并结合在一起,形成更长的DNA链,从而引发一种反应免疫反应.这种反应不仅杀死了癌细胞,而且阻止了癌变组织的进一步生长。这种方法不同于传统的抗癌药物治疗,有望开创药物开发的新时代。
遗憾的是,癌症是一个众所周知的全球健康问题,目前的治疗方法有其局限性。然而,基于核酸(即DNA和RNA,携带重要信息的分子)的药物可以控制细胞的生物功能,并有望改变医学的未来,为克服癌症和其他由病毒和遗传疾病引起的难以治疗的疾病提供重大推动。
东京大学的一个研究小组,由工程研究生院的助理教授Kunihiko Morihiro和Akimitsu Okamoto教授领导,受到启发,使用人造DNA创造了一种新的抗癌药物。冈本说:“我们认为,如果我们能创造出一种与传统药物作用机制不同的新药,它们可能对迄今为止无法治疗的癌症有效。”
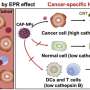
核酸类药物的使用癌症治疗一直具有挑战性,因为很难使核酸区分癌细胞和其他健康细胞。这意味着,如果健康的细胞在不经意间受到攻击,就有可能对患者的免疫系统产生不利影响。然而,这是该团队第一次能够开发出一种发夹状的DNA链,它可以激活一种自然免疫反应,以靶向并杀死特定的癌细胞。
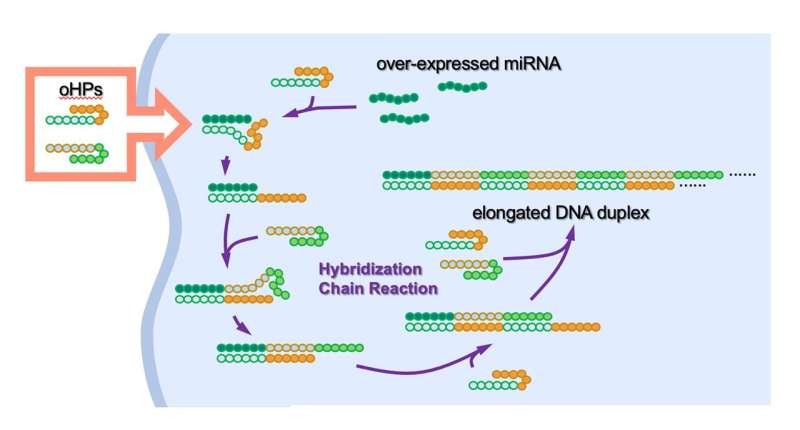
癌细胞可以过度表达或复制过多的特定DNA或RNA分子,导致它们不能正常工作。该团队创造了被称为oHPs的人工溶瘤(杀死癌症)发夹DNA对。当这些oHPs遇到一种称为miR-21的短(微)RNA时,它们被触发形成更长的DNA链,miR-21在一些癌症中过表达。
通常情况下,由于其弯曲的发夹形状,oHPs不会形成更长的线。然而,当人工oHPs进入细胞并遇到目标microRNA时,它们会打开并与之结合并形成更长的链。这随后导致免疫系统识别出过表达的miR-21的存在是危险的,并激活先天免疫反应,最终导致细胞死亡癌症细胞.
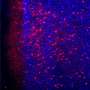
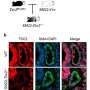
这些测试对在人宫颈癌源性细胞、人三阴性乳腺癌源性细胞和小鼠恶性黑色素瘤源性细胞中发现的过表达miR-21有效细胞.冈本说:“该研究小组发现,由于短DNA oHPs和过表达miR-21之间的相互作用,形成了长DNA链,这是其用作选择性免疫扩增反应的第一个例子,可以靶向肿瘤回归,提供了一类新的核酸候选药物,其机制完全不同于已知的核酸药物。”
“这项研究的结果对医生、药物研发研究人员和癌症患者来说都是好消息,因为我们相信它将为他们的药物开发和用药政策提供新的选择。接下来,我们将以这一研究结果为基础进行药物开发,并详细研究药物的疗效、毒性和潜在的给药方法。”
这篇论文发表在美国化学学会杂志.在治疗方法问世之前,这项研究还有很多步骤要走,但研究小组对其益处充满信心核酸为新药物发现.