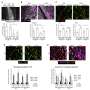
为了阻止癌症扩散,研究人员瞄准了两个触发新血管生长的信号开关
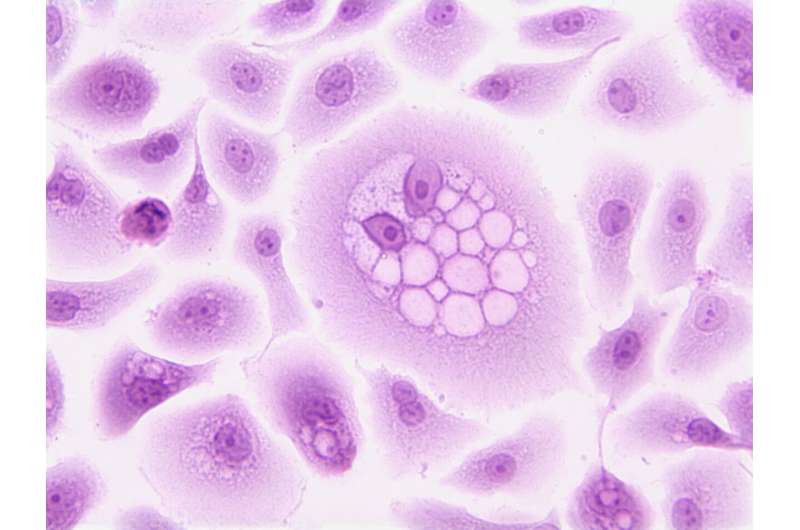
根据东安格利亚大学和Quadram研究所的最新研究,同时达到两个目标可能是阻止侵袭性癌症扩散的关键。
研究人员发现,肿瘤的生长在小鼠中,可以通过同时瞄准两个触发新血管生长的信号开关来停止。
他们的研究发表在该杂志上癌症研究通讯,指出了治疗人类癌症的新方法。
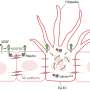
没有一个血液供应为了提供氧气和营养,肿瘤不能长到几毫米以上。在生长过程中,它们释放信号蛋白,触发细胞形成血管,这一过程被称为血管生成。
破坏这些信号蛋白和细胞表面上识别它们的受体之前已被确定为减缓肿瘤生长的潜在策略,但目前这种干预措施的临床效益显示出有限的成功,除非辅以化疗。
在某种程度上,这是因为研究人员仍然不确定在健康状态下或癌症中控制血管生成的确切机制。第一个被称为血管内皮生长因子(VEGF)的信号蛋白组在1970年被发现,但直到20世纪90年代末,才发现了VEGF共受体家族-这些是神经蛋白酶-1和2。
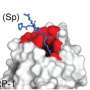
共受体是位于细胞表面它们在哪里识别和结合信号蛋白.神经蛋白酶1和2与vegf结合,以及大量其他蛋白质,在细胞内触发级联信号以激活血管生成。因此,在癌症中停止这一过程可以防止肿瘤发展成复杂的组织血管他们需要成长。
研究人员一直在尝试这样做,使用癌症的细胞和动物模型来确定阻断神经蛋白酶与VEGF相互作用的化合物。事实上,针对神经蛋白酶-1的候选药物已经被证明可以减缓小鼠乳腺癌的进展。
然而,迄今为止,同时针对神经蛋白酶1和2的研究有限。Christopher Benwell博士是一名博士后研究员,与Stephen Robinson博士在Quadram研究所的团队合作,他试图通过研究神经蛋白酶1和2的基因或两者的组合被删除的小鼠来解决这一理解上的差距。
他们发现,在多种癌症模型中,同时靶向neuropilin-1和2会严重抑制肿瘤血管生成、癌症生长和转移,也就是说,它会扩散到其他次要部位。重要的是,这种效应的程度比单独针对其中一种受体时要大得多。
“我们对这些结果感到非常兴奋,并开始深入研究如何操纵这些受体来控制血管生成在不同的疾病状态下,”克里斯托弗·本维尔博士说。
对培养细胞的进一步研究揭示了这种保护是如何起作用的。当两种神经素受体都被靶向时,VEGF受体会被细胞迅速破坏,从而从源头上切断血管生成反应。
“我们希望这项研究能激励其他人考虑靶向多种蛋白质的影响,以实现协同抗癌反应。通过这样做,我们的目标是限制a癌症东英吉利大学生物科学学院的斯蒂芬·罗宾逊博士说。