这一发现可以解释为什么女性更容易患老年痴呆症
斯克里普斯研究所和麻省理工学院(MIT)的科学家们发现了阿尔茨海默病的分子原因的线索——这条线索也可以解释为什么女性患这种疾病的风险更高。
这项研究于2022年12月14日报告科学的进步研究人员发现,与死于阿尔茨海默病的男性相比,死于阿尔茨海默病的女性大脑中存在一种特别有害的、经过化学修饰的炎症免疫蛋白补体C3,其含量要高得多。他们还表明,雌激素——在绝经期产量下降——通常可以防止这种形式的补体C3的产生。
“我们的新发现表明,补体系统的一个组成部分的化学修饰有助于导致阿尔茨海默病,并可能解释,至少在部分上,为什么这种疾病主要影响女性,”该研究的资深作者斯图尔特·利普顿说,他是医学博士,斯克里普斯研究所分子医学系教授和步骤家庭基金会捐赠主席,也是加州拉霍亚的临床神经学家。
这项研究是与Steven Tannenbaum博士领导的团队合作进行的,他是麻省理工学院生物工程、化学和毒理学安德伍德-普雷斯科特教授。
阿尔茨海默氏症是随着年龄增长而发生的最常见的痴呆症大约600万人仅在美国。它总是致命的,通常在发病后的十年内,目前还没有批准的治疗方法可以阻止疾病的发展,更不用说逆转它了。治疗方法的缺陷反映了一个事实,即科学家从未完全了解阿尔茨海默病是如何发展的。科学家们也不完全清楚为什么女性占了近三分之二的病例。
利普顿的实验室研究生物化学和分子事件神经退行性疾病,包括形成修饰型补体c3的化学反应,这一过程被称为蛋白质s -亚硝基化。Lipton和他的同事们之前发现了这种化学反应一氧化氮(NO)相关分子紧密结合在蛋白质的特定氨基酸构建块上的硫原子(S),形成修饰的“sno蛋白”。由NO等小原子簇修饰的蛋白质在细胞中很常见,通常会激活或使a失活靶蛋白的功能。由于技术原因,s -亚硝基化比其他蛋白质修饰更难研究,但Lipton怀疑这些蛋白质的“sno风暴”可能是阿尔茨海默氏症和其他神经退行性疾病的关键因素。
在这项新研究中,研究人员使用了检测s -亚硝基化的新方法来量化40例死后修饰的蛋白质人类的大脑.一半的大脑来自于死于阿尔茨海默氏症的人,另一半来自于没有死于阿尔茨海默氏症的人——每组男性和女性平均分配。
在这些大脑中,科学家们发现了1449种被s -亚硝基化的不同蛋白质。在最常以这种方式修饰的蛋白质中,有几种已经与阿尔茨海默病有关,包括补体C3。引人注目的是,与男性相比,女性阿尔茨海默病患者大脑中s -亚硝基化C3 (SNO-C3)的水平高出6倍多。
补体系统是人类免疫系统中进化较早的部分。它由包括C3在内的一系列蛋白质组成,这些蛋白质可以相互激活,从而引发炎症,这被称为“补体级联”。30多年前,科学家们就已经知道,与神经正常的大脑相比,阿尔茨海默氏症的大脑具有更高水平的补体蛋白和其他炎症标志物。最近的研究特别表明,补体蛋白可以触发被称为小胶质细胞的常驻大脑免疫细胞破坏突触——神经元之间传递信号的连接点。许多研究人员现在怀疑,这种破坏突触的机制至少在一定程度上是阿尔茨海默病过程的基础,而突触的丧失已被证明是阿尔茨海默病大脑认知能力下降的重要相关因素。
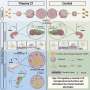
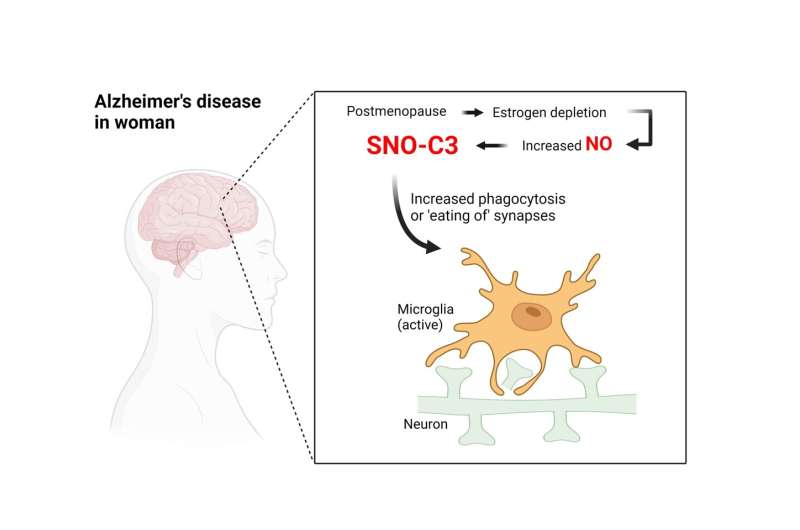
为什么SNO-C3在患有阿尔茨海默症的女性大脑中更常见?长期以来,有证据表明,女性荷尔蒙雌激素在某些情况下可以起到保护大脑的作用;因此,研究人员假设雌激素可以特别保护女性的大脑免受C3 s -亚硝基化的影响——当雌激素水平随着绝经期急剧下降时,这种保护就失去了。用人工培养的人脑细胞进行的实验支持了这一假设,结果显示SNO-C3随着雌激素(β-雌二醇)水平的下降而增加,这是由于一种生成NO的酶的激活大脑细胞。SNO-C3的增加激活了突触的小胶质细胞破坏。
利普顿说:“为什么女性更容易患阿尔茨海默氏症一直是个谜,但我认为我们的研究结果代表了这个谜题的重要部分,从机械上解释了女性随着年龄增长而更易患病的原因。”
他和他的同事们现在希望用去亚硝基化化合物(去除SNO修饰)进行进一步的实验,看看它们是否能减少阿尔茨海默氏症动物模型的病理,并最终减少人类的病理。
“基于异常的阿尔茨海默病女性优势的机制洞察蛋白质C3的s -亚硝基化”,由麻省理工学院的杨红梅、Haitham Amal、John Wishnok、Sarah Lewis和Steven Tannenbaum共同撰写;以及斯克里普斯研究所的吴昌基、艾米丽·沙赫勒、多莉特·特鲁德勒、中村智宏和斯图尔特·利普顿。