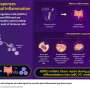
表观遗传紧急开关提高防御感染
在感染期间,造血系统从正常模式切换到紧急模式。这提高了对病原体的防御能力。德国癌症研究中心的科学家们现在在小鼠的血液干细胞和祖细胞中发现了一种表观遗传开关,可以触发从一种模式到另一种模式的切换。
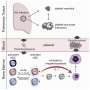
如果体内启动了紧急造血程序,这表明免疫系统处于警报状态,并有两个不同的目的:与“正常模式”的造血相比,紧急造血程序导致在感染或炎症期间消耗的免疫细胞的补充增加。此外,应急程序使整个免疫系统进入预激活状态,有助于更快地清除感染。
应急方案的特点是,例如,增加的分割率血液干细胞成熟白细胞的平衡向骨髓细胞(巨噬细胞和粒细胞)倾斜。通常,紧急程序是由病原体的典型分子成分或促炎信使物质(如某些干扰素)触发的。
但是在血液干细胞中发生了什么祖细胞?有没有启动紧急程序的手机开关?德国癌症研究中心的Nikolaus Dietlein和Hans-Reimer Rodewald领导的科学家针对一种特殊的表观遗传修饰,简称H2Bub1。
它参与了病毒感染后由干扰素激活的基因的开启,这对癌症非常重要国防对感染。这种修饰,附着在DNA的包装蛋白上,组蛋白,被USP22酶再次去除。
H2Bub1和USP22是触发血液干细胞紧急程序的开关吗?由罗德瓦尔德领导的研究人员对血液干细胞USP22基因关闭的小鼠进行了研究。在这些动物中,具有所有关键特征的造血紧急程序运行时没有任何可检测到的感染或干扰素水平的增加。
转基因动物比正常小鼠更能抵御单核增生李斯特菌的感染。此外,他们血液中重要的清道夫细胞,中性粒细胞,更能成功地吞噬细菌。
不出所料,遗传物质在基因修饰动物的血细胞中也有明显更多的表观遗传H2Bub1修饰。“H2Bub1水平的升高似乎是报警按钮,把免疫系统待命。特别是,这使得先天免疫防御,这在与病原体的初步接触中特别重要,处于高度防御警戒状态,”当前出版物的第一作者Nikolaus Dietlein说。USP22去除H2Bub1修饰后,在正常动物中终止警报。
H2Bub1和USP22也在人类细胞根据目前的研究,它们的功能与小鼠相当。
Hans-Reimer Rodewald说:“在老鼠身上,我们能够证明表观遗传修饰提高了对疾病的防御能力感染.然而,USP22的缺失如何影响人类造血干细胞和祖细胞仍是未知的,现在应该进行研究。药物对USP22的抑制有一天可能有助于提高对病原体的免疫防御能力。然而,到目前为止,这还没有得到证实,需要在进一步的研究中进行测试。”
研究结果发表在该杂志上科学免疫学.