FDA批准基因疗法治疗难治性膀胱癌

患有高风险膀胱癌的患者现在有了一种新的治疗方法。
美国食品和药物管理局已经批准了一种基因治疗叫做Adstiladrin,它的作用是病人谁有所谓的高风险非肌肉侵入性手术膀胱癌(NMIBC)没有对标准做出回应治疗例如,芽孢杆菌Calmette-Guérin (BCG),但尚未扩散。卡介苗是一种典型的结核病疫苗。
FDA生物制品评估和研究中心主任彼得·马克斯博士在一份机构新闻稿中说:“这项批准为医疗保健专业人员提供了一种创新的治疗方案,用于对卡介苗治疗无反应的高风险NMIBC患者。”“今天的行动解决了一个迫切需要的领域。FDA仍然致力于促进安全有效的药物的开发和批准癌症治疗方法。”
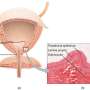
在新诊断的膀胱癌患者中,约有75%至80%已经穿透膀胱内膜生长,但尚未侵入肌肉。约30%至80%的病例复发并有扩散风险。治疗通常包括切除肿瘤并使用卡介苗来降低癌症复发的风险。
但是对于那些对卡介苗没有反应的癌症患者来说,这种方法很少治疗方案。
患者将每三个月通过导尿管接受一次Adstiladrin。
根据美国疾病控制和预防中心的数据,每年约有5.7万名男性和1.8万名女性被诊断出患有膀胱癌。在美国,每年约有1.2万名男性和4700名女性死于这种疾病。
FDA官员基于157名患者的多中心临床研究批准了Adstiladrin,其中98名患者患有没有扩散的bcg无反应性疾病。
患者每三个月接受一次Adstiladrin治疗,持续12个月或直到治疗毒性过大。在接受Adstiladrin治疗的患者中,约51%的患者癌症症状消失。中位缓解期为9.7个月。有反应的患者中,约46%的患者在至少一年的时间内完全缓解。
与Adstiladrin相关的最常见的不良反应是膀胱排出、疲劳、膀胱痉挛、尿急、尿血、畏寒、发热、排尿痛。FDA表示,免疫抑制或免疫缺陷的人不应使用Adstiladrin。
更多信息:美国癌症协会有更多相关报道膀胱癌。
2022每日健康。版权所有。