小鼠研究提出了减少癌症幸存者心血管疾病的新治疗策略
纽约纪念斯隆·凯特琳癌症中心(MSKCC)的研究人员发现,常见的癌症治疗方法,如放疗或蒽环类药物,通过激活关键的炎症信号通路,对心脏组织造成长期损害。这项研究发表在《科学》杂志上实验医学杂志(杰姆)的研究表明,抑制这一途径可以降低癌症幸存者在晚年患心脏病的几率。
许多癌症都是用辐射和/或药物来治疗的肿瘤细胞通过破坏它们的DNA但这些治疗也会损害患者健康细胞的DNA。随着癌症患者的存活率不断上升,其长期后果越来越受到关注。
例如,放射治疗或一类被称为蒽环类的dna破坏药物可能会对心脏产生延迟的毒性作用,增加患心血管疾病的风险,包括冠状动脉疾病或心力衰竭。一项研究发现,在霍奇金淋巴瘤的长期幸存者中,心血管疾病的发生率比普通人群高5倍。
“DNA损伤导致多年后晚期组织毒性的机制癌症治疗我们对其知之甚少,”MSKCC的放射肿瘤学家亚当·m·施密特(Adam M. Schmitt)说。“确定毒性的致病机制及其激活的早期生物标志物将为干预治疗以预防毒性提供机会。”
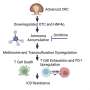
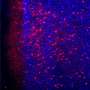
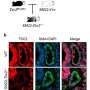
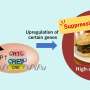
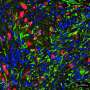
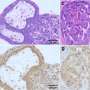
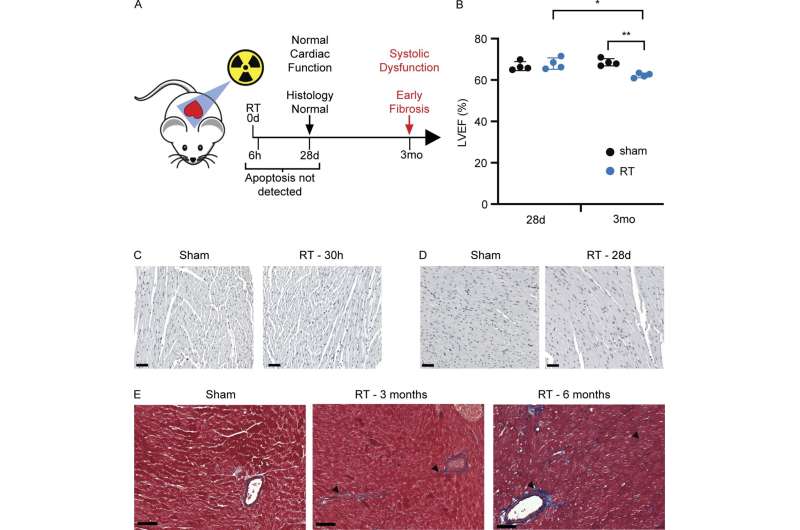
在他们的研究中,Schmitt和同事们发现,在小鼠暴露于辐射或蒽环类药物一个月后,一种被称为成纤维细胞的特定心脏细胞群激活了一组基因,促进了与病病性炎症和组织纤维化相关的各种免疫细胞类型的招募。在3-6个月内,小鼠出现了心脏功能障碍的迹象,到12个月时,许多小鼠死于心力衰竭。
研究人员确定,这一病理过程是由一种称为cGAS-STING途径的免疫信号通路驱动的。这一途径通常促进炎症反应的DNA片段病原菌但是,Schmitt和他的同事推断,它也可能被辐射或蒽环类药物治疗产生的DNA片段激活。
缺乏cGAS或STING蛋白的小鼠可以免受dna损伤性癌症治疗的毒副作用。他们没有出现心脏炎症的迹象,心脏功能保持正常,治疗一年后仍然存活。STING蛋白的一种小分子抑制剂也能保护小鼠免受毒性作用放射治疗或蒽环类药物。
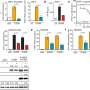
通过研究乳腺癌患者Schmitt和他的同事发现证据表明cGAS-STING通路可能在人类心脏毒性中发挥同样重要的作用。cGAS-STING信号诱导的关键炎症蛋白之一是CXCL10,研究人员发现,在蒽环素治疗后CXCL10水平增加最多的患者随后出现了与心脏毒性相关的超声心动图变化。
Schmitt说:“综上所述,我们的数据显示,靶向cGAS-STING途径作为一种预防dna损伤性癌症治疗的心脏并发症的治疗方法具有巨大的潜力。”这些数据表明了这一点临床试验使用cGAS-STING抑制剂来预防dna损伤性癌症治疗后的心血管疾病是有必要的。”