利用光来控制神经元的兴奋性
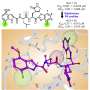
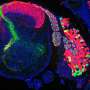
![Optogenetic polymerization and assembly of electrically functional materials in cells. (A) Photosensitizer proteins (PS) are expressed in the cytosol of the genetically specified neuron types. Upon light irradiation (hν) and introduction of polymer monomers, photosensitizer proteins locally generate singlet oxygen (<sup>1</sup>O2)after instersystem crossing (ISC), which polymerizes and assembles conductive or insulating polymers in the cell and on the cell membrane, modulating the membrane capacitance and excitability (V<sub>m</sub>, membrane potential). (B and C) Merged confocal fluorescence (left) and transmitted light (TL; right) images of fixed human embryonic kidney (HEK) 293T cells coexpressing dTomato (red) and miniSOG (green) after 7 min of irradiation in the presence of 1 mM DAB [labeled as poly(3,3′-diaminobenzidine) (PDAB<sup>+</sup>)] (B) and 1 mM aniline and 1 mM N-phenyl-p-phenylenediamine (PPD) [labeled as photopolymerized polyaniline (PANI<sup>+</sup>)] (C). White dashed lines represent the boundary of irradiation formed by the epifluorescence light source; Hoechst 33342 nuclear stain is shown in blue; all scale bars are 50 µm. (D) PDAB and PANI depositions were quantified by measuring the pixel brightness of cells in the TL images and normalizing it to the average background of the cell-free parts of the image. Values represent means ± SEM; unpaired, two-tailed t tests. ****P = less than 0.0001. (E and F) Merged confocal fluorescence and TL images of fixed rat cortical neurons expressing miniSOG (miniSOG<sup>+</sup> neurons) after 7 min of irradiation in the presence of 1 mM DAB (E) and 1 mM aniline and 1 mM PPD (F). (G and H) Corresponding images of neurons expressing only mCherry (miniSOG<sup>−</sup> neurons). (I and J) Insulating (I) and conductive (J) polymer deposition quantified as described in (D). ns, not significant. Credit: <i>Science Advances</i> (2022). DOI: 10.1126/sciadv.ade1136 利用光来控制神经元的兴奋性](https://scx1.b-cdn.net/csz/news/800a/2022/using-light-to-manipul.jpg)
近20年前,科学家们发明了通过照射神经元来刺激或抑制神经元的方法。这种被称为光遗传学的技术,使研究人员能够发现特定神经元的功能,以及它们如何与其他神经元通信以形成电路。
在这种技术的基础上,麻省理工学院和哈佛大学的研究人员现在已经设计出一种方法来实现长期的变化神经元活动.有了新策略,他们可以利用曝光改变神经元细胞膜的电容,从而改变它们的兴奋性(它们对电信号和生理信号的反应有多强或多弱)。
神经元兴奋性的变化与大脑中的许多过程有关,包括学习和衰老,也在一些大脑疾病中观察到,包括阿尔茨海默病。
“这种新工具旨在以光可控和长期的方式上下调节神经元的兴奋性,这将使科学家们能够直接建立各种神经元类型的兴奋性与动物行为之间的因果关系,”麻省理工学院托马斯D.和弗吉尼亚卡伯特化学助理教授、麻省理工学院和哈佛大学布罗德研究所的成员小王说。“我们的方法在疾病模型中的未来应用将告诉我们,微调神经元的兴奋性是否有助于将异常的大脑回路重置为正常。”
王和哈佛大学工程与应用科学学院的助理教授刘佳是这篇论文的资深作者,该论文发表在今天的《科学》杂志上科学的进步.
Chanan Sessler,麻省理工学院化学系研究生;博德研究院博士后周一鸣;和哈佛大学研究生王文博是这篇论文的主要作者。
膜处理
光遗传学是科学家用来操纵神经元活动的工具,通过工程神经元来表达光敏离子通道。当这些经过改造的神经元暴露在光线下时,通过通道的离子流动的变化会抑制或促进神经元的活动。
“通过使用光,你可以打开或关闭这些离子通道,这反过来会刺激或沉默神经元。这允许实时快速响应,但这意味着如果你想控制这些神经元,你必须不断地照亮它们,”Sessler说。
麻省理工学院和哈佛大学的研究小组着手修改这项技术,使其能够产生更持久的兴奋性变化,而不是短暂的激活或抑制活动。为了做到这一点,他们专注于改变细胞膜的电容,这是细胞膜导电能力的关键决定因素。
当电容的时候细胞膜神经元变得不那么兴奋——也就是说,不太可能对来自其他细胞的输入做出反应而激发动作电位。当电容降低时,神经元变得更容易兴奋。
“神经元的兴奋性由两种膜特性控制:电导率和电容。虽然许多研究都集中在离子通道执行的膜导电性上,但自然发生的髓鞘形成过程表明,调节膜电容是在大脑发育、学习和衰老过程中调节神经元兴奋性的另一种有效方法。所以,我们想知道是否可以通过改变细胞膜来调节神经元的兴奋性电容刘说。
在斯坦福大学做博士后的时候,刘和他的同事们证明了他们可以通过诱导神经元在细胞膜上组装导电或绝缘聚合物来改变神经元的兴奋性。在2020年发表的那项研究中,刘使用了一种称为过氧化物酶的酶来组装聚合物。但是,这种方法没有考虑到精确控制在聚合物聚集的地方。这也带来了一些风险,因为该反应需要过氧化氢,而过氧化氢会损害细胞。
为了克服这些限制,刘在哈佛大学的实验室与王在麻省理工学院的实验室合作,尝试了一种新的方法。研究人员没有使用过氧化物酶,而是使用了一种经过基因工程改造的光敏蛋白,这种蛋白可以催化聚合物的形成。
研究人员利用在实验室培养皿中培养的神经元,改造细胞,使其表达这种被称为miniSOG的光敏蛋白。当被蓝色波长的光激活时,miniSOG会产生称为活性氧的高活性分子。与此同时,研究人员将细胞暴露在导电聚合物(称为PANI)或绝缘聚合物(称为PDAB)的构建块中。
在几分钟的光照下,活性氧刺激这些积木组装成PDAB或PANI。
使用一种称为全细胞膜片钳的技术,研究人员发现,具有导电PANI聚合物的神经元变得不那么兴奋,而具有绝缘PDAB聚合物的神经元变得更兴奋。他们还发现,长时间的光照会产生更大的兴奋性变化。
“光遗传聚合的优势是对聚合反应的精确时间控制,这允许可预测的膜性能的逐步微调,”周说。
持久的变化
研究人员表明,兴奋性的变化持续了三天,这是他们在实验室培养皿中保持神经元存活的时间。他们现在正致力于改进这项技术,使其能够用于脑组织切片,然后,他们希望,在动物的大脑中,如老鼠或秀丽隐杆线虫。
研究人员说,这样的动物研究有助于阐明神经元兴奋性的变化是如何影响多发性硬化症和阿尔茨海默病等疾病的。
王文博说:“如果我们知道某个神经元群体在某种特定疾病中具有较高或较低的兴奋性,那么我们就可以通过将这些只在该神经元类型中表达的光敏蛋白之一转导给小鼠来调节该神经元群体,然后看看这是否对行为产生预期的影响。”“在不久的将来,我们更多地将其作为研究这些疾病的模型,但你可以想象潜在的治疗应用。”
本文转载自麻省理工学院新闻(web.mit.edu/newsoffice/),这是一个很受欢迎的网站,涵盖有关麻省理工学院研究、创新和教学的新闻。