发现了视力丧失的潜在新机制
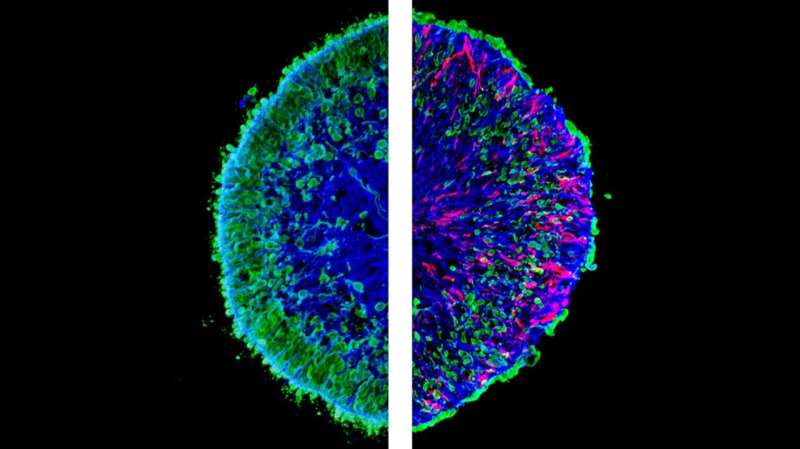
人类视网膜上的视觉细胞可能不会在某些疾病中简单地死亡,而是事先被机械地从视网膜上转移出去。来自德国
在他们的研究中,他们使用了实验室生产的微型人类视网膜,即所谓的类器官。在新一期的杂志上自然通讯,他们报告了他们的发现,这为全新的研究方法铺平了道路,特别是在与年龄相关的黄斑变性(AMD)相关的研究中。
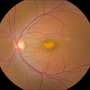
这种被称为细胞挤压的原理尚未在美国被研究过神经退行性疾病该研究小组负责人迈克·卡尔教授说。在德国,黄斑变性是导致失明和严重视力损害的主要原因。据估计,60岁以上的人中有四分之一患有老年性黄斑变性。黄斑是黄斑内的一个特殊区域人的视网膜这是高分辨率色觉所需要的。在黄斑变性中,数以千计的光敏视觉细胞,即所谓的光感受器细胞,在黄斑中丢失。
“这是我们研究项目的起点:我们观察到光感受器丢失了,但我们无法检测到任何光感受器细胞死亡在视网膜迈克·卡尔(Mike Karl)解释道,他在德国德累斯顿工业园区(DZNE)和德累斯顿工业大学(TU Dresden)的CRTD进行研究。“10天内,视网膜类器官中一半的光感受器消失了,但显然它们并没有在视网膜中死亡。这让我们很好奇。”
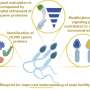
研究人员——DZNE和CRTD以及亥姆霍兹环境研究中心(UFZ)都参与其中——开始了对原因的详细研究。这让他们在2012年进行了一项研究:来自伦敦国王学院的乔迪·罗森布拉特(Jody Rosenblatt)是第一个描述活细胞挤压的人——细胞从上皮中机械喷射出来。
由此挤压出来的细胞只能相继死亡。她在肾脏的简单上皮细胞中证实了这种机制。迈克·卡尔和他的团队现在在他们的开创性工作中表明,这种挤压也可以在更复杂的视网膜上触发,视网膜由几种不同的细胞类型组成,并导致神经变性。有趣的是,这种细胞挤压可以解释之前在AMD和其他疾病患者的老化和病变视网膜中报道的外围细胞,但直到现在还没有详细研究。
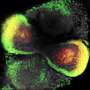
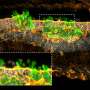
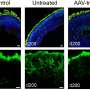
研究人员利用了他们之前开发的一项技术:他们研究所谓的视网膜类器官——一种在实验室中由人类干细胞培养出来的类似器官的人类视网膜三维模型。这些类器官提供了人类黄斑的一些特征。研究小组发现,先前在各种神经退行性疾病中描述的两种物质——蛋白质HBEGF和tnf——足以引发视网膜变性瀑样.
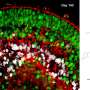
在这个过程中,研究人员通过所谓的实时成像实时拍摄类器官,这被认为是细胞跟踪的黄金标准。“我们能够在实验室里通过细胞挤压捕捉到光感受器的退化,”迈克·卡尔说。科学家们发现,这种挤压是由PIEZO1蛋白的激活引发的,PIEZO1是一种生物力学力的传感器。
生物力学可能在视网膜变性中发挥更大的作用是一项新发现。“视网膜不像肌肉一样是生物力学上活跃的组织。众所周知,神经系统疾病与细胞形状的变化有关,但生物力学调节剂在多大程度上参与其中尚未得到详细研究,”卡尔说。
多亏了类器官,他和他的团队能够以一种加速的方式观察到这一过程,可以这么说:虽然光感受器在患者体内消失需要几年甚至几十年的时间,但这样的过程现在可以在实验室里只需要40天就能重现。在下一步,研究人员现在想要找出这种机制是否以与类器官相同的方式发生在人类患者身上。最初的研究结果表明,这可能是相同的机制,但仍然缺乏证据。
在他们的研究中,德累斯顿的研究人员还发现,在他们的模型的实验环境中,药物可以防止挤压。他们使用一种特殊的蛇毒来阻断细胞上的机械传感器PIEZO1。结果,不仅光感受器没有被射出,而且视网膜的进一步病理变化也被阻止了。迈克·卡尔说:“这给未来复杂神经退行性疾病(如AMD)的预防和治疗带来了希望。”