参与脊髓小脑性共济失调的新蛋白质提供了对选择性神经元脆弱性的洞察
像阿尔茨海默氏症和帕金森氏症这样的神经退行性疾病是由于突变蛋白的异常积累而导致特定类型神经元的损失。虽然在这些疾病中,已经发现特定的大脑区域特别脆弱,但大脑细胞和区域对有毒突变蛋白的这种差异脆弱性的原因和确切机制尚不清楚。
贝勒医学院杰出服务教授、德克萨斯儿童医院Jan and Dan Duncan神经学研究所(Duncan NRI)创始主任Huda Zoghbi博士的实验室最近的一项研究,在1型脊髓小脑共济失调(SCA 1)的背景下解决了这个问题,并揭示了导致这种神经退行性疾病的分子参与者和途径的多样性。
这一发现发表在神经元,为更好地理解其他神经退行性疾病的区域脆弱性绘制了研究路径。
SCA1是一种进行性神经退行性疾病,全世界每10万人中就有1到2人患病,主要特征是丧失运动协调和平衡能力。它是由一种名为聚谷氨酰胺(polyQ)重复序列的突变ATXN1蛋白的存在引起的。
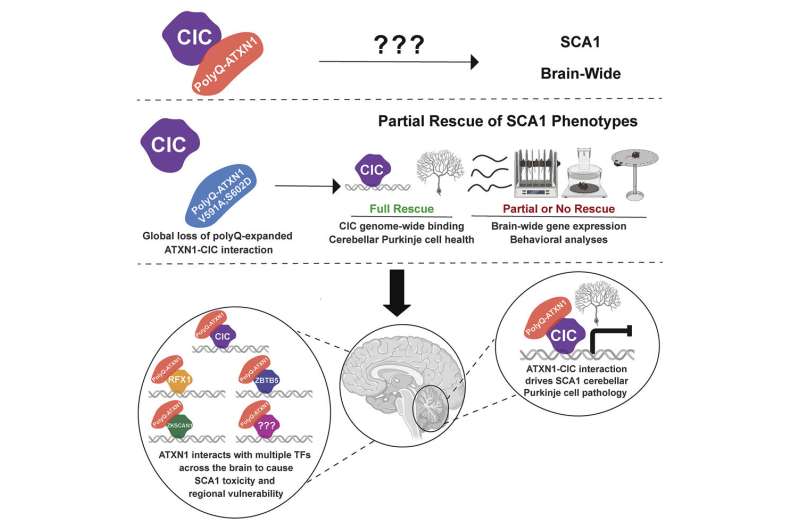
在健康神经元中,ATXN1与capicua (CIC)相互作用,CIC是一种抑制几种基因表达的蛋白质。另一方面,当突变ATXN1与CIC结合时,CIC靶基因高表达,最终对神经元产生毒性。先前的研究表明,SCA1小鼠模型中小脑浦肯野细胞的所有变化都源于ATXN1-CIC复合物活性的增强。
然而,ATXN1蛋白广泛表达并在脑的各个区域发挥作用大脑.
Zoghbi说:“令人惊讶的是,一个尚未探索的关键问题是,是否CIC在其他大脑区域中驱动ATXN1的毒性,或者是否其他分子玩家在其他受影响的神经元中驱动毒性。”Zoghbi也是霍华德休斯医学研究所的研究员。
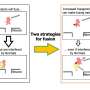
为了解决这个问题,Zoghbi实验室的研究生斯蒂芬妮·科芬(Stephanie Coffin)生成了一个新的SCA1小鼠模型来模拟人类ATXN1突变及其在整个大脑中的影响。在这个模型中,ATXN1基因有一个扩展的聚谷氨酰胺延伸,但她也使这两个基因发生了突变氨基酸这对ATXN1-CIC相互作用至关重要。
Zoghbi团队发现,这两种突变完全削弱了ATXN1-CIC在所有大脑区域的相互作用。
“ATXN1-CIC复合物的破坏导致了SCA1的部分改善神经系统症状比如运动不协调、呼吸和寿命短,只让一部分基因表达变化恢复正常,”科芬说。
“总之,这些发现为我们提供了一个线索,CIC可能不是驱动SCA1的唯一ATXN1相互作用者,其他分子参与者可能有助于SCA1患者和动物模型中出现的各种神经症状的发展和进展。”
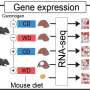
为了确定ATXN1的其他相互作用体,他们使用免疫沉淀和质谱进行了无偏倚蛋白质组学筛选。
“鉴于转录变化是SCA1的标志,我们专注于在人类和小鼠大脑的不同区域表达的三种转录因子,称为ZKSCAN1, ZBTB5和RFX1,”科芬补充说,他目前是Pelagos制药公司的神经科学项目经理。
“我们验证了ATXN1与这些新发现的伙伴之间的相互作用,并发现RFX1和ZKSCAN1调控的基因表达在SCA1小鼠和人类神经元中发生了改变。此外,这两个新发现的伙伴- rfx1和zkscan1 -以及CIC预计可以调节约33%的基因,这些基因在SCA1小鼠模型中表达发生改变,突出了它们在这种疾病的发病机制中发挥的重要作用。”
Zoghbi说:“我们非常惊讶地发现,对于这种单基因疾病,突变蛋白使用不同的伙伴来驱动不同脑细胞的毒性。”“事实上,这项研究强调了研究其他疾病驱动蛋白的伙伴的重要性,不仅对其他聚谷氨酰胺疾病,而且广泛地对所有神经退行性疾病。只有通过这样的系统研究,我们才能了解导致这些疾病的机制,才能更好地探索治疗干预措施。”
更多信息:Stephanie L. Coffin等,ATXN1- cic复合物的破坏揭示了额外的核ATXN1相互作用在脊髓小脑性共济失调1型中的作用,神经元(2022)。DOI: 10.1016 / j.neuron.2022.11.016