埃博拉疫苗的安全性和免疫原性试验取得了可喜的结果
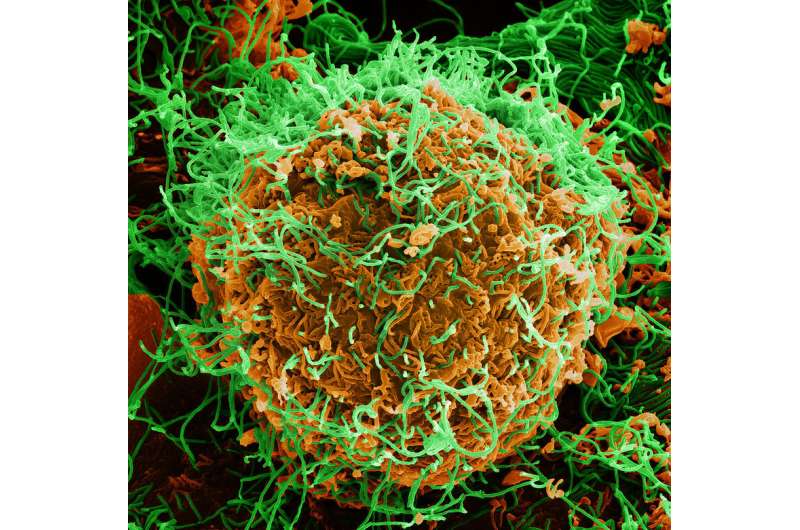
埃博拉疫情在撒哈拉以南非洲各国周期性发生。虽然已有针对扎伊尔埃博拉病毒种的疫苗,并已通过世卫组织资格预审,但必须继续并加强努力补充现有数据,以制定针对成人和儿童的安全有效的埃博拉疫苗战略。
PREVAC国际联盟,包括来自Inserm和非洲、美国和英国机构的科学家,发表了在西非进行的大规模随机临床试验的结果新英格兰医学杂志.这些结果证实了三种不同疫苗方案的安全性,并提示免疫反应可诱导并维持长达12个月。
在许多撒哈拉以南非洲国家经常面临埃博拉疫情的背景下,疫苗被视为对抗疾病传播的核心工具。自2019年以来,两种疫苗获得了世卫组织针对扎伊尔埃博拉病毒种的资格预审:由默克、夏普和多梅公司开发的疫苗rVSVΔG-ZEBOV-GP和Ad26。ZEBOV和MVA-BN-Filo疫苗方案由强生公司提供。
除了这些进展之外,埃博拉疫苗的研究必须继续进行。的确,需要更多的数据,以便就不同类别的人口使用这些疫苗提出最适当的建议。
测试了三种疫苗方案
这是PREVAC国际联盟的目标。从2017年开始,一项大规模、多中心、随机、安慰剂对照的二期试验动员了非洲、欧洲和美国的研究团队在利比里亚、几内亚、塞拉利昂和马里共同工作。这是迄今为止在成人和1岁及以上儿童中进行的规模最大的埃博拉疫苗接种试验之一。
该试验旨在测量三种不同的埃博拉疫苗方案产生的免疫反应的速度、强度和持久性,涉及上述疫苗。它还评估了所使用的各种产品的安全性和耐受性。
- 试验的第一种疫苗方案包括注射一剂Ad26。56天后,ZEBOV注射了一剂MVA-BN-Filo。
- 第二个方案包括注射一剂rVSVΔG-ZEBOV-GP。
- 最后,第三个方案以一剂rVSVΔG-ZEBOV-GP开始,56天后再用同样的剂量疫苗作为助推器。
总的来说,这项试验包括1400名成年人和1401名年龄在1到17岁之间的儿童,他们被随机分为几个组来测试和比较三种方案与安慰剂。
获得的数据表明,这三种方案在成人和儿童中都是安全的,耐受性良好。在接种疫苗后和随后的7天内,大多数参与者报告了注射部位疼痛和其他轻微症状(发烧、肌肉和关节疼痛、头痛等),这些症状通常在7天后消失。
这三种方案也产生了快速增加,14天后,的数量抗体针对病毒,在第一次疫苗接种后1至3个月达到峰值。虽然目前还不能确定这是否免疫反应预防感染,目前的科学文献表明,这些抗体的数量与对病毒的保护水平之间存在很强的相关性。这些抗体在第一次注射后12个月就被检测出来了。
该试验的首席研究员Yazdan Yazdanpanah解释说:“在这项临床试验期间收集的数据很有价值,因为它们有助于确认现有疫苗的安全性和潜在有效性,从而有可能在扎伊尔埃博拉病毒流行和流行间期对高危人群改进疫苗接种建议。”
首席研究员Mark Kieh解释说:“由于该领域所有专业人员的坚定参与,以及人们对研究的坚持,这项试验的特点是参与者保留率很高。”
“PREVAC试验是国际研究新发和再发感染的一个真正成功的例子。我们表明,通过建立在牢固伙伴关系基础上的坚实合作,我们可以在世界上受该疾病影响最严重的地区推进埃博拉研究,”NIAID临床研究和特别项目副主任H Clifford Lane说。