2023年1月24日功能
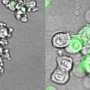
癌细胞是如何死亡的:科学家探索凋亡的杀手亲属焦亡的新途径
对于任何学过生物学101的人来说,凋亡的概念——程序性细胞死亡——在课程的早期就被教授了。不了解细胞是如何死亡的,就无法了解细胞的生命周期。
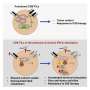
生物101课程中通常不会教的是细胞死亡的另一种方式,一种叫做焦亡的过程,一种炎症和坏死形式的细胞死亡主要包括癌症细胞.在化疗过程中,细胞凋亡可转变为焦亡。对于接受化疗的患者来说,细胞凋亡不仅会转化为焦亡,这个过程还可以帮助激活免疫系统。焦亡的启动和免疫系统的激活都是通过特定的蛋白质途径介导的。
迄今为止,大多数研究都将化疗诱导的焦亡与一种称为gasdermin E的中介蛋白联系起来,它通常被认为是这一过程中的唯一刽子手。然而,一轮有趣的研究已经深入研究了焦亡的过程,揭示了触发这种形式的程序性细胞死亡的新分子途径。
一系列新颖的研究中出现了新的发现,这些研究挑战了关于细胞在化疗影响下死亡方式的主流科学智慧。这项研究通过扩大参与这种形式的细胞死亡的蛋白质途径的可能数量,为化学癌症治疗中的焦亡提供了新的线索,并暗示未来可能还会发现其他途径。
俄亥俄州凯斯西储大学(Case Western Reserve University)医学院的病理学家周伯文(Bowen Zhou)博士领导了这项新研究,他提供了关于焦亡的实践经验,解释说:“在化疗的反应中,凋亡细胞死亡的诱导可以转化为一种称为焦亡的溶解性细胞死亡。”
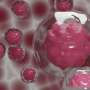
术语“溶细胞死亡”,或“细胞裂解”,指的是由细胞最外层膜不可挽回的损伤引起的细胞分解。当细胞内的物质从洞中溢出时,细胞就无法存活,这就是焦亡的原因。它是瘀伤和暴力的,目的是细胞死亡。在焦亡过程中,分子反应的级联冲击细胞膜上的大孔,不可逆转地破坏稳定,并最终破坏细胞。
凯斯西储研究小组进一步认为,要想化疗产生效果,它必须触发导致细胞死亡的生物途径。科学家们优雅的研究,包括分析血液和骨髓活检的患者急性髓系白血病,为了解在化疗影响下引发焦亡的多种途径打开了一扇新的窗口。
“焦亡是一种程序性坏死细胞死亡的机制,由gasdermins介导,gasdermins是一种形成孔隙的蛋白质家族,”周教授说,他是血液癌症焦亡论文的主要作者。这项研究发表在该杂志上科学的信号,强调了在广泛使用的化疗药物的影响下可能导致细胞死亡的几种孔隙形成途径。
除了在通过焦亡导致癌细胞死亡中起作用外,形成孔隙的gasdermins是一个蛋白质家族,也与免疫反应有关。其中一种蛋白质,gasdermin D,在由激活caspase-1的炎性小体的形成诱导的癌细胞死亡中起着主导作用。但是,焦亡的故事显然不是始于和结束于气素D或它的近亲气素e。科学家们说,这是一个比其他研究报告复杂得多的分子传奇。
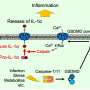
“Caspase-1在炎症条件下激活gasdermin D,而caspase-3在凋亡条件下激活gasdermin E,例如化疗诱导的条件下,”Zhou断言。“这些途径被认为是分开的。
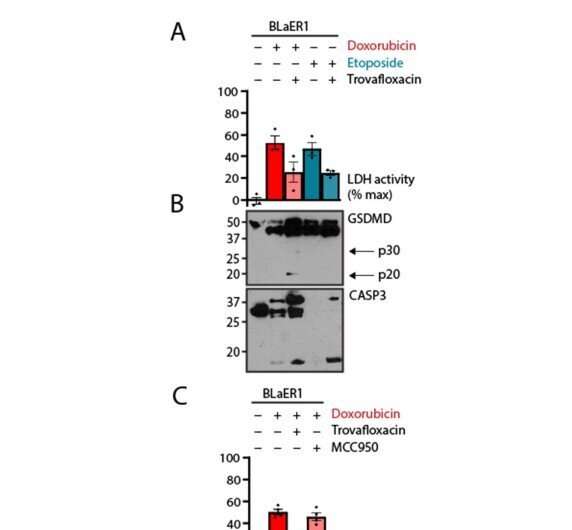
“然而,我们发现它们是使焦性细胞死亡的综合看门人网络的一部分。我们观察到气皮素D是体外培养的主要焦化介质血细胞对阿霉素和依托泊苷这两种常见的造血恶性肿瘤化疗的反应。”
说句题外话,为了说明气皮素在健康和疾病中的复杂程度,另一种气皮素蛋白,气皮素A,以及气皮素D,也与自身免疫性疾病和某些癌症有关。然而,正如凯斯西部研究的复杂细节所报道的那样,gasdermin蛋白因其形成孔隙的能力而值得注意,特别是在化疗的影响下。
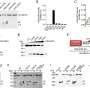
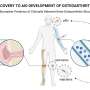
周和同事们的研究揭示了多种导致癌细胞死亡的途径,为研究焦化途径提供了新的见解——这是与主流科学智慧相悖的立场。尽管高丰度的gasdermin E具有主导作用,但人髓系细胞向焦亡的转化可以通过跨膜蛋白pannexin-1(也称为PANX1通道)独立介导。这是通过诱导一个依赖于气皮素D或完全独立于气皮素的交替焦化途径发生的。
在15名白血病患者的血液和骨髓活组织检查中,gasdermin E、gasdermin D和PANX1的相对丰度可以预测通路会引起化疗后的焦性细胞死亡
从这项研究中得到的信息是多焦点的:癌细胞不会仅仅因为暴露于化疗而死亡。它们通过一种编程机制死亡,这种机制可以通过几种信号通路中的任何一种进行。Zhou和他的同事们也充分证明了化疗期间的焦亡不仅仅依赖于gasdermin e。通过研究暴露于化疗中的人类髓细胞,科学家们发现焦亡也可以通过PANX1进行。即使面对挑战教条的研究,可能还有其他尚未被发现的孔隙形成途径。
“下一步,仔细解剖孔隙形成蛋白的作用将是至关重要的,包括那些尚未涉及的,在血液病和其他恶性肿瘤中,以定制适当的治疗反应,”Zhou总结道。
更多信息:周博文等,Gasdermins和pannexin-1介导化疗诱导的造血恶性肿瘤细胞裂解途径,科学的信号(2022)。DOI: 10.1126 / scisignal.abl6781
©2023科学BOB体育赌博X网络