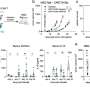
研究人员发现新型CRISPR基因剪刀

像人类一样,细菌和古生菌也会受到病毒的攻击。这些微生物已经发展出自己的免疫防御策略来对抗病原体。细菌防御,如CRISPR-Cas系统,具有不同的蛋白质和功能,帮助细菌保护自己免受外来入侵者的侵害。
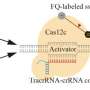
这种防御是基于一种共同的机制:CRISPR核糖核酸(crRNA),作为“向导RNA”,帮助检测外源基因组的区域,如病毒的DNA,以进行靶向切割。由crRNA引导的crispr相关核酸酶(Cas)可以像剪刀一样切割其目标:这是人类在许多技术中利用的一种自然策略。
Chase Beisel说:“考虑到不同的核酸酶已经很好地转化为新的和改进的技术,这一领域的任何发现都可能给社会带来新的好处。”他在Würzburg Helmholtz rna感染研究所(HIRI)描述了他的实验室的研究动机。该研究所是与Julius-Maximilians-Universität (JMU)在Würzburg合作的布伦瑞克亥姆霍兹感染研究中心的一个站点。
Beisel与美国密苏里州本森希尔公司(Benson Hill, Inc.)的Matthew Begemann和犹他州立大学(Utah State University)的Ryan Jackson共同发起了目前对一套特定CRISPR-Cas系统的研究。研究结果发表在该杂志上自然与此同时,由德克萨斯大学的瑞恩·杰克逊和大卫·泰勒领导的另一个团队进行了详细的结构分析。
与其他已知的CRISPR核酸酶不同
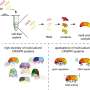
“我们正在探索最初与Cas12a聚集在一起的CRISPR核酸酶,这种核酸酶通过识别和切割侵入性DNA来保护细菌。一旦我们发现了更多的,我们就意识到它们与Cas12a有足够的不同,可以进行更深入的研究,”该研究的第一作者Oleg Dmytrenko说。“这一探索使我们发现,这些被我们称为Cas12a2的核酸酶不仅与Cas12a有很大的不同,而且与任何其他已知的CRISPR核酸酶也有很大的不同。”
最关键的区别在于防御行动的机制。当Cas12a2识别侵入性RNA时,核酸酶将其裂解,但也可以破坏细胞内的其他RNA和DNA,损害其生长并限制感染的扩散。HIRI博士后Oleg Dmytrenko说:“一般来说,这种阻止感染的防御策略在细菌中已经被发现。”“其他一些CRISPR-Cas系统也是这样工作的。然而,基于crispr的防御机制依赖于单个核酸酶来识别入侵者并降解细胞DNA和RNA,这在以前还没有被观察到。”
详细的发现
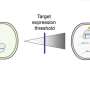
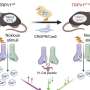
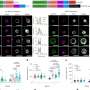
的蛋白质序列Cas12a2的结构和区别于Cas12a。Cas12a2被一个原间隔区侧翼序列(PFS)激活,识别与引导RNA互补的目标RNA。靶向RNA触发侧链核酸切割,从而降解RNA、单链DNA和双链DNA。这种活动导致细胞停滞,可能是通过破坏细胞中的DNA和RNA,从而损害生长。Cas12a2可用于分子诊断和RNA生物标记物的直接检测,这已被原理证明。
毁灭性的裂痕
在另一个团队对核酸酶的进一步结构分析中他们在同一期的自然Cas12a2在免疫反应的不同阶段与RNA靶标结合后,发生了重大的结构变化。这反过来又导致核酸酶出现一个暴露的裂缝,它可以粉碎它遇到的任何核酸——无论是RNA、单链DNA还是双链DNA。该研究还发现了使Cas12a2突变的方法,以改变核酸酶在识别其RNA目标后降解的核酸。这些细节为未来开辟了潜在的广泛技术应用。
更多信息:Chase Beisel, Cas12a2通过rna触发的dsDNA破坏引发流产感染自然(2023)。DOI: 10.1038 / s41586 - 022 - 05559 - 3.www.nature.com/articles/s41586 - 022 - 05559 - 3
大卫·泰勒,RNA靶向释放CRISPR-Cas12a2任意核酸酶活性,自然(2023)。DOI: 10.1038 / s41586 - 022 - 05560 - w.www.nature.com/articles/s41586 - 022 - 05560 - w