在对抗无法治愈的癌症方面的一个有希望的发现
来自肯特大学和格林尼治大学合作的梅德韦药学院(MSOP)的研究人员与来自Inselspital(伯尔尼大学医院,瑞士)和奥尔登堡大学(德国)的同事合作,最近发现了对抗癌症治疗的人类蛋白质是如何工作的。
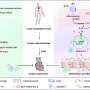
半乳糖凝集素-9是一种存在于所有哺乳动物体内的蛋白质,负责调节人类的免疫反应。由于它能够抑制t细胞的抗癌活性而引起特别的兴趣,t细胞是一种白细胞,是免疫系统的一部分,可用于帮助对抗癌症。因此,半乳糖凝集素-9被癌细胞用来逃避免疫监视。
攻克半乳糖凝集素-9使t细胞和其他抗癌疗法无效的能力——或者至少进一步了解这是如何发生的——可以帮助更多的癌症被治愈。
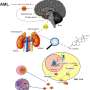
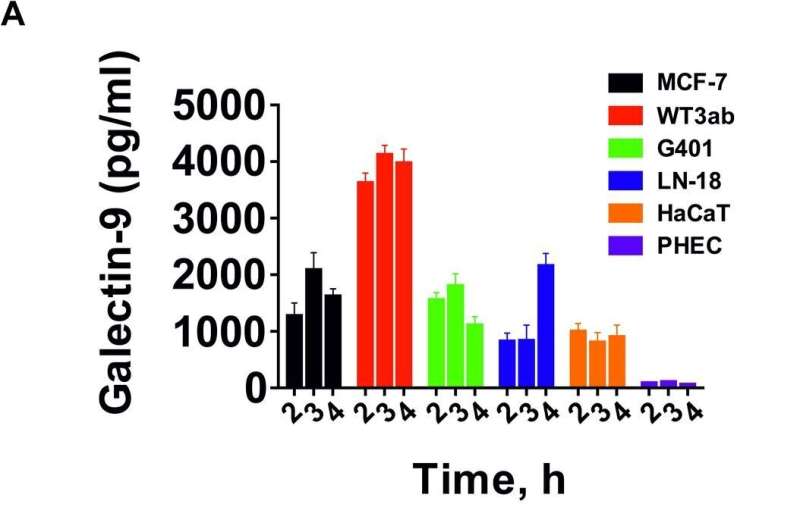
先前的研究表明,半乳糖凝集素-9在大量人类癌症中高度表达,包括非常侵袭性的肿瘤,如胶质母细胞瘤——一种侵袭性癌症,5年生存率低于10%,可能发生在大脑或大脑脊髓以及更常见的癌症,如乳腺癌和肺癌。然而,已知静止状态下的实体肿瘤细胞要么分泌少量的半乳糖凝集素-9,要么在大多数情况下根本不分泌半乳糖凝集素-9。
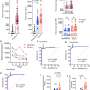
该团队开始阐明T细胞是否可以诱导来自实体恶性肿瘤的人类癌细胞分泌半乳糖凝集素-9,以及与细胞表面蛋白相比,这种可溶性形式是否表现出更高的全身免疫抑制活性。
这项研究首次表明,t细胞在不同类型的人体内诱导半乳糖凝集素-9的分泌癌症细胞来源于实体恶性肿瘤的生化机制差异。这些发现强调了半乳糖凝集素-9在抗癌免疫逃避中的关键作用,并强调了进一步研究半乳糖凝集素-9及其调控途径的必要性,以便为大量癌症(包括目前通常无法治愈的癌症)开发新的有效治疗方法。
进行这项研究的研究联盟领导人、MSoP研究主任Vadim Sumbayev博士说:“这些结果不仅证实了我们对这种抗癌蛋白质的已知知识,而且还帮助我们更好地了解它的功能以及它如何与其他类型的肿瘤起作用。”
“了解半凝集素-9和整个抗癌免疫逃避机制将使我们能够绘制这些途径,并通过简单的生化标记测试快速识别每个患者的这些途径,并使现有或新的治疗方法更有效。”
“此外,这些知识将使我们能够在个性化的基础上确定最佳的治疗靶点,并设计出高效的药物,以所需的方式与它们相互作用。结果,对每个人来说癌症病人我们将能够迅速适应高效和负担得起的个性化靶向免疫疗法。这将显著改善两者存活率以及癌症患者治疗期间和治疗后的生活质量。虽然还有很长的路要走,但这让我们离开发拯救生命的癌症治疗方法更近了一步。”
这项工作发表在癌症免疫治疗杂志.
更多信息:Stephanie Schlichtner等人,T淋巴细胞诱导来源于实体恶性肿瘤的人类癌细胞分泌半乳糖凝集素-9,与其他免疫检查点蛋白合作促进免疫抑制,癌症免疫治疗杂志(2023)。DOI: 10.1136 / jitc - 2022 - 005714